Introducción
El síndrome de desmielinización osmótica abarca los términos correspondientes a mielinólisis pontina y extrapontina.(1)(2) Se refiere al daño severo de la cubierta mielínica neuronal con sintomatología neurológica variada, que refleja el daño de los tractos motores descendentes.(1)(3) En esta patología los oligodendrocitos y la mielina se ven afectados.(4) Además, pueden verse afectados corteza, sustancia blanca, sustancia gris, puente, núcleos caudados y putamen.(5) La mielinólisis central pontina es la presentación clásica, que refleja una gran susceptibilidad de la sustancia blanca pontina a esta condición.(6) Años atrás se consideraba una entidad de descarte solo verificable en necropsia, sin embargo, con la aparición de nuevos estudios imagenológicos, específicamente nuevas opciones en resonancia magnética de cerebro, existe un incremento de casos detectados. A propósito del diagnóstico mencionado presentamos neuroimágenes de esta patología y un breve comentario sobre el desequilibrio hidroelectrolítico causal.
Caso clínico
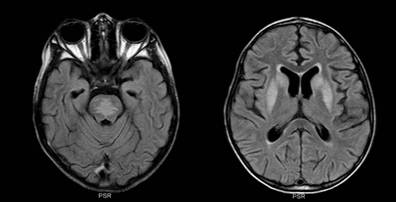
Se trata de un escolar de 10 años masculino que ingresa a nuestra unidad por complicaciones postquirúrgicas de peritonitis (bridas y adherencias). A su ingreso registra hiponatremia 113mEq/dL que fue manejada con reposiciones en 2 ocasiones hasta llevarlos a 130mEq/dL en un intervalo de 24 horas (17mEq). A la semana de hospitalización presenta hipoactividad, disminución de la fuerza muscular, arreflexia, afasia, disfagia, sialorrea, alteración del sensorio con periodos de irritabilidad y somnolencia, agresividad y hemiplejía izquierda. Se realiza tomografía computarizada (TC) de cráneo en la que se observan imágenes hipondesas pontinas (ver Figura 1), ante sospecha de síndrome de desmielinización osmótica se solicita resonancia magnética (RM) de cerebro que reporta imágenes hipointensas bilaterales a nivel de las cabezas de los núcleos caudados y putamen en T1 con zonas correspondientes hiperintensas en T2 y flair, a nivel de puente de Variolo hipointensidad en T1 con alta señal en T2 y flair, ligera dilatación de ventrículos laterales (índice de Evans 0.32) compatibles con manifestaciones pontinas y extrapontinas del síndrome de desmielinización osmótica (SDO), con tratamiento de soporte el paciente evoluciona favorablemente, presentando una recuperación total del estado neurológico (ver Figuras 2 y 3). (Figura 1)(Figura 2)(Figura 3)
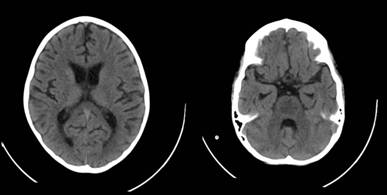
Figura 1 Tomografía de cerebro: Se observan imágenes hipodensas a nivel de puente y ganglios de la base.
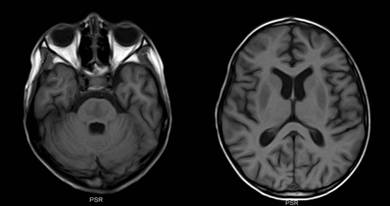
Figura 2 IRM de cerebro T1: Se observan imágenes hipointensas a nivel de cabeza de los núcleos caudados y putámen. Imágenes hipointensas en puente de Variolo.
Discusión
Aunque la mayoría de casos de SDO se describen en pacientes con estados hiperosmolares y trasplantados hepáticos, se ha descrito también en casos de hipofosfatemia, hipokalemia, hepatitis, enfermedad renal crónica, hemodiálisis, hiperemesis gravídica, anorexia nerviosa, diabetes, enfermedad de Wilson, leucemia, linfomas, quemados severos, entre otros. (1)(3)(5) Kinoshita 2018 reporta el caso de un adolescente con cetoacidosis diabética que desarrollo SDO de causa multifactorial.(7) Vladimirov et al. reportan el caso de un adulto con bulimia con alteraciones electrolíticas por vómitos que desarrolla SDO a pesar de correcciones lentas. (8)
La sintomatología del SDO incluye tetraparesia espástica, parálisis pseudobulbar, coma y convulsiones. (1) La presentación clásica del SDO se denomina síndrome “locked in”, cuadro caracterizado por cuadriplejía, anartria, capacidad para seguir estímulos con los ojos, pero no seguir órdenes y signo de Babinski positivo bilateral. (3) El coma puede ocurrir en el 15% de los casos de SDO. (6) Además se describen trastornos del comportamiento como falta de control en los impulsos, descontrol emocional, agresividad, falta de concentración, síndromes depresivos, catatonia, mutismo y labilidad emocional. (2)
La etiología es multifactorial, aunque usualmente se la relaciona con la corrección agresiva de hiponatremia, la cual se reporta hasta en el 67% de las ocasiones, también se han encontrado casos en pacientes con niveles normales o ligeramente disminuidos de sodio, o que han sido repuestos con rangos aceptables de sodio. (9) Se cree que se debe al estrés hiperosmótico que se da durante la rápida corrección de la hiponatremia, que causa una ruptura de la barrera hematoencefálica, posiblemente debido a la incapacidad del endotelio que expone a los oligodendrocitos a factores mielinolícos que no suelen estar en contacto con el cerebro. (3)
A pesar de que la patogénesis exacta se desconoce, varios mecanismos han sido propuestos como causa única o procesos combinados entre los que destacan la deshidratación de los oligodendrocitos que da como resultado la separación de los axones de su capa mielínica con la subsecuente mielinólisis y necrosis, la apoptosis oligodendrocítica causada por el estrés metabólico durante los eventos de deshidratación osmótica y la acumulación de sustancias mielinotóxicas macrofágicas que potencian la desmielinización. (9)
Con relación a la hiponatremia, se denomina así a la concentración de sodio plasmático menor a 135 mEq/L, aunque se define de forma arbitraria como clínicamente significativa aquella por debajo de 130 mEq/L. Las manifestaciones clínicas que se relacionan a la disfunción del sistema nervioso central (SNC) se suelen relacionar a valores menores a 125 mEq/L. (10)
De forma general no se debe corregir más de 10-12 mEq/L/día de sodio excepto en hiponatremias de instalación rápida documentada. La corrección brusca de la hiponatremia, puede desarrollar desmielinización osmótica uno a varios días después. (10)
Previamente esta patología se identificaba solo en necropsias, pero con la introducción de la RM muchos casos de SDO oligosintomáticos o asintomáticos se han podido detectar. (2)(3)(9) Los cambios en la TC o RM se evidencian entre 2 y 7 días posteriores a la aparición de los signos clínicos. (10) La RM es el test confirmatorio de SDO. (2)(3)(6) La RM muestra imágenes hiperintensas pontinas en T2 con restricción a la difusión manifestada como incremento de la señal en DWI y disminución de la señal en ADC. (3) Las localizaciones extrapontinas pueden ubicarse en cerebelo, unión cortical de la sustancia gris con la sustancia blanca, tálamo, subtálamo, amígdala, globo pálido, putamen, núcleo caudado y cuerpos geniculados laterales, esta variedad de localizaciones es la que explica la variedad de síntomas. (3)(6)(9) El diagnóstico de SDO no se puede excluir con neuroimágenes normales y la severidad de las lesiones no se relacionan con la severidad clínica, curso o pronostico del paciente. (9)
En la TC las áreas lesionadas suelen presentar hipodensidad con ocasional realce al contraste durante fases tardías, sin embargo, debido a los artefactos (Hounsfield’s lines) su sensibilidad es baja. (2)(6) Los hallazgos en RM usualmente son claros entre 1 a 6 meses, sin embargo, algunos pueden ser tan temprano como 3 semanas. (9) Diffusion weighted imaging (DWI) es el mejor método para identificar de forma temprana cambios asociados a SDO, reportando estudios anormales hasta 24 horas después del inicio de los síntomas comparado con RM clásica que lo suele mostrar a las 2 semanas. (9) Las imágenes halladas son el reflejo de los cambios de líquido intra y extra celulares, así DWI es una técnica relativamente nueva y muy sensible al movimiento de moléculas de aguda, ha sido muy útil en el diagnóstico precoz de SDO. La clínica suele preceder a los cambios en IRM. (4)
La anatomía patológica del SDO se describe clásicamente como áreas simétricas de desmielinización a nivel pontino y extrapontino que incluyen sustancia gris y blanca del puente, cerebelo, amígdala, tálamo, globo pálido, putamen, núcleo caudado y cuerpos geniculados laterales. Estas lesiones inician en el centro del puente y se distribuyen de forma triangular a manera las alas de una mariposa. Se ven con mayor frecuencia en esta localización debido a que hay un mayor entrecruzamiento de sustancia gris y blanca, frecuentemente un anillo de tejido normal envuelve las lesiones. (9)
Conclusiones
El síndrome de desmielinización osmótica es un diagnóstico que debe ser considerado en pacientes con sintomatología neurológica de aparición subaguda y antecedentes de trastornos de la osmolaridad plasmática, sobre todo aquellos que incluyan el sodio sérico. En el tratamiento de la hiponatremia, no exceder la velocidad de reposición recomendada de más de 10 a 12 mEq de sodio en 24 horas. Ante esta posibilidad y considerando las condiciones clínicas, el estudio de neuroimagen es necesario. Una vez establecido el diagnóstico se debe proporcionar el tratamiento adecuado de la patología de base, vigilar la evolución e incluir manejo multidisciplinario que incluya terapia física y rehabilitación.