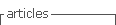Estimada editora:
La pandemia provocada por un nuevo coronavirus ha puesto a prueba a la comunidad médica mundial. Varios estudios han identificado los factores de riesgo para desarrollar un cuadro clínico severo-crítico por este nuevo agente. Este riesgo en los pacientes con esclerosis múltiple podría estar incrementado debido al uso de medicamentos inmunosupresores o inmunomoduladores. El reporte del primer caso de enfermedad por coronavirus en el Ecuador, ha hecho que se planteen medidas prácticas y objetivas dirigidas a los médicos encargados del manejo de este grupo de pacientes así como también recomendaciones para los pacientes en este contexto.
En diciembre de 2019 se reportaron por primera vez en la ciudad de Wuhan (China) un grupo de pacientes con neumonía de etiología desconocida. Semanas después el agente etiológico fue identificado, logrando comprobar que se trataba de un nuevo coronavirus al cual se lo nombró SARS-CoV-2 y al cuadro clínico asociado al mismo se lo denominó COVID-19 (coronavirus disease). Rápidamente el virus se propagó, confirmándose casos positivos fuera de China y comprometiendo otros continentes. A finales de enero de 2020 ya se habían reportado casos positivos en al menos 19 países, incluyendo Norteamérica. (1)(2)
COVID-19 en el Ecuador
El primer caso de COVID-19 fue reportado por el Ministerio de Salud Pública (MSP) del Ecuador el 29 de febrero de 2020, y el día 11 de marzo de 2020 la Organización Mundial de la Salud (OMS) declaró a COVID-19 como una pandemia.
Al momento de redactar el presente trabajo (5 de abril de 2020), Ecuador suma 3646 casos con 180 decesos por esta enfermedad. El 69.2% (n=2524) se concentran en la provincia de Guayas, el 9.5% (n=345) en Pichincha, el 4.3% (n=158) en la provincia de Los Ríos y el 2.7% (n=99) en la provincia de Azuay. El 55% (n=2009) son hombres y el 60% (n=2184) de los casos se encuentran en edades comprendidas entre los 20 a 49 años. (3)
Los trabajos publicados sobre COVID-19 describen un curso leve de la enfermedad en el 81% de los pacientes, mientras el 19% podría desarrollar un cuadro severo-crítico. (4)(1) Se han descrito varios factores de riesgo para desarrollar una enfermedad severa, los cuales incluyen: ser adulto mayor, obesidad, tabaquismo y tener comorbilidades entre ellas enfermedades cardiovasculares, diabetes mellitus, enfermedades pulmonares y cáncer. (5)
Esclerosis Múltiple en el Ecuador
Hasta el momento se desconoce si las personas con esclerosis múltiple (EM) tienen un riesgo mayor de infectarse o de desarrollar una enfermedad grave, ya sea por su condición per se o por la necesidad de tratamiento con fármacos inmunomoduladores o inmunosupresores. (5)
El Ecuador es un país de baja prevalencia de EM (3 a 5 casos por 100.000 habitantes) teniendo al momento 346 pacientes diagnosticados: 168 en Quito, 126 en Guayaquil, 48 en Cuenca y 4 en Manabí. La edad promedio de los pacientes se encuentra entre los 20 a 49 años, según los estudios reportados en cada ciudad. (6)(7)
Esclerosis múltiple en el Ecuador y su relación con COVID-19
Las ciudades donde se encuentran los hospitales de referencia para el tratamiento de EM, coinciden como podemos ver, con las provincias más afectadas por la pandemia, siendo los centros que atienden pacientes con EM ahora los encargados del manejo de pacientes con COVID-19. (Figura 1)
Es por esto que el objetivo del presente documento es presentar recomendaciones para la atención y el manejo terapéutico de los pacientes con EM ante la situación epidemiológica actual.
Estas recomendaciones se basan en la mejor evidencia disponible al momento, en opinión de expertos y en la posición de varias entidades encargadas de investigación y tratamiento de este grupo de pacientes en la región y en zonas de alta prevalencia. Las mismas pueden modificarse en función de nueva información, de las circunstancias especiales de cada paciente y de la situación epidemiológica de nuestro país. Se aclara que las presentes recomendaciones no están dirigidas para población pediátrica ni mujeres embarazadas, ya que la evidencia al momento es insuficiente para estos grupos poblacionales.
Los pacientes con EM deben acoger las recomendaciones realizadas para la población general dadas por la OMS y el MSP, que incluyen:
-Lavarse las manos con frecuencia con agua y jabón o usar un desinfectante a base de alcohol (durante al menos 20 segundos)
-Evitar tocarse los ojos, la nariz y la boca
-Cubrir su boca y nariz con el codo flexionado o con un pañuelo de papel al toser o estornudar. El pañuelo usado debe desecharse de inmediato.
-Mantener una distancia mínima de 1 metro entre personas
-En caso de presentar fiebre, tos o dificultad para respirar, buscar atención médica
-Evitar el consumo de productos animales crudos o poco cocinados.
-Limpiar y desinfectar los objetos o superficies que se tocan frecuentemente usando un producto común de limpieza doméstico (alcohol, cloro o detergente)
Adicionalmente, los pacientes con EM deben seguir las siguientes recomendaciones. (8)
-Evitar las visitas, reuniones públicas y las multitudes
-Evitar utilizar el transporte público
-Siempre que sea posible, se debe usar una alternativa (telemedicina o llamadas telefónicas) para evitar acudir de forma presencial a sus citas médicas de control.
-Los centros encargados de proveer del tratamiento a los pacientes deberán dar las facilidades para que el retiro de la medicación la realice un familiar siguiendo las medidas de prevención ya descritas para la población general
-Cumplir con aislamiento preventivo estricto, especialmente aquellos pacientes que reciben tratamientos de moderada y alta eficacia.
Recomendaciones sobre los fármacos modificadores de la enfermedad (FME) disponibles en Ecuador en las siguientes posibles situaciones:
1. Pacientes con reciente diagnóstico de EM.
El inicio de tratamiento debe ser individualizado y analizado caso por caso. Algunos FME (Fingolimod, Alemtuzumab, Cladribine) pueden producir una disminución del recuento linfocitario, lo que podría significar un mayor riesgo de complicaciones en caso de infección por COVID-19, conociendo de antemano que la linfopenia se ha asociado a un incremento en el riesgo de mortalidad por COVID-19.(4)(9) Este riesgo debe ser balanceado con el beneficio de iniciar una medicación, si el cuadro es agresivo o con factores de mal pronóstico, (10) se debe considerar el uso de un tratamiento de rescate como corticoide y aplazar el inicio de fármacos de alta eficacia. Cabe recalcar que los estudios sobre las características clínicas de EM en nuestro país no evidencian un comportamiento agresivo de la misma en la gran mayoría de los pacientes. (6)
En pacientes sin un cuadro agresivo y sin factores de mal pronóstico, se recomienda iniciar el tratamiento con medicamentos como Acetato de Glatiramer, Interferón o Teriflunamida ya que no producen inmunosupresión. (11)
2. Pacientes con EM que reciben acetato de Glatiramer o Interferones sin infección por COVID-19.
Los pacientes con estas terapias deben continuar con las mismas. El interferón B1a incluso podría tener un efecto terapéutico antiviral en pacientes con COVID-19, por lo que no se debería suspender el tratamiento, salvo en los casos que hubiese una linfopenia significativa (complicación muy rara). (12)(13)
3. Pacientes con EM que reciben tratamiento a base de Fingolimod o Siponimod sin infección por COVID-19.
Se debe individualizar los casos y buscar posibles factores de riesgo para desarrollar COVID-19 severa como edad, obesidad, comorbilidades adicionales, ya que debido a su mecanismo de acción, estos FME pueden producir linfopenia. Los pacientes en los cuales después de valorar el riesgo y beneficio se continúe con el tratamiento, deberán seguir las recomendaciones para pacientes con linfopenia significativa (uso de mascarilla).
Hay que tener presente que la suspensión de estos fármacos por tiempos relativamente prolongados puede producir reactivación de la enfermedad. (14) Por lo tanto se debe continuar con el tratamiento. El criterio para suspensión de Fingolimod por linfopenia es de ≤200 linfocitos por mL.
4. Pacientes con EM que reciben tratamiento con anticuerpos monoclonales anti CD20 como Rituximab u Ocrelizumab sin infección por COVID-19
Se recomienda retrasar la siguiente dosis del fármaco anti CD20 hasta que pase la epidemia. Las células CD19+ tardan en normalizarse hasta 9-12 meses luego de la administración de Rituximab. En los datos disponibles sobre Ocrelizumab, la mediana de tiempo que demoraron los pacientes para recuperar los niveles de células CD19+ fue de 72 semanas. (15)
5. Pacientes con EM que reciben tratamiento con Natalizumab sin infección por COVID-19
Se recomienda postergar la administración de la nueva dosis hasta 8 semanas, ya que no aumenta el riesgo de recaídas. Hay que tener presente que la suspensión de este fármaco por tiempos relativamente prolongados puede producir reactivación de la enfermedad. (14)
6. Pacientes con EM que reciben tratamiento con terapias de inducción como Alemtuzumab y Cladribine, sin infección por COVID-19
Si el paciente ha recibido su primera dosis de Alemtuzumab se recomienda retrasar la segunda dosis hasta que el riesgo de infección por coronavirus haya pasado. Hay que recordar que el riesgo de infecciones virales es mayor en los tres a seis meses después de la dosis de Alemtuzumab. Los datos disponibles demuestran que un intervalo de hasta 18 meses entre la primera y segunda dosis de Alemtuzumab es segura, sin riesgo de reactivación de la enfermedad. (16)
Los datos son menos claros para Cladribine, al ser una terapia de reciente uso a nivel mundial, sin embargo, los estudios demuestran que se lo puede clasificar como un fármaco de riesgo intermedio, ya que depleta de una forma relativamente pobre a los linfocitos T, siendo más sensibles los linfocitos T CD4+ que los CD8+. En el estudio de fase III del fármaco, las infecciones virales fueron poco frecuentes después de Cladribine. Cladribine se administra en dos semanas al año separadas por un mes, en el segundo año el esquema es el mismo. (5) Por lo tanto, la recomendación actual sería que si el paciente inició la primera semana de tratamiento, debe completarse el primer ciclo.
7. Pacientes con EM y diagnóstico de COVID-19
Se deben individualizar los casos. Los pacientes en uso de terapias como Interferón y Acetato de Glatiramer pueden continuar su tratamiento. Como se ha mencionado, el interferón puede tener un efecto antiviral en aquellos pacientes con COVID-19 severa.(5) Para el resto de FME, se recomienda la suspensión de la medicación y reanudarlos cuando el paciente esté asintomático y tenga tres pruebas de PCR (reacción en cadena de la polimerasa) para SARS-Cov2 negativas, realizadas con una semana de diferencia.
8. Pacientes con EM y recaída
Se debe descartar en primera instancia una pseudo-recaída. De confirmar que se trata de una recaída, se recomienda valorar la severidad de la misma. Si es sensitiva o leve y no compromete la funcionalidad, el paciente puede permanecer en casa y observar la evolución manteniendo un seguimiento estrecho sin recibir tratamiento, tomando en cuenta que la mayoría de las recaídas de la EM son seguidas de algún grado de recuperación espontánea incluso sin tratamiento. (17)
En caso de que se compruebe una recaída moderada, se recomienda el uso de corticoides a altas dosis por vía intravenosa u oral, los estudios han demostrado que los esteroides orales son menos costosos (serían fáciles de conseguir para el paciente) y no menos efectivos que los esteroides intravenosos. Los esteroides pueden ser administrados en domicilio sin requerir la asistencia a los hospitales o centros de infusión. Al no disponer de metilprednisolona vía oral en el país, se recomienda un régimen diario de 25 tabletas de 50 mg de prednisona o 32 tabletas de 6 mg de dexametasona por 3 a 5 días. Está demostrado que la reducción paulatina de las dosis luego de este curso breve no es necesaria, ya que un pulso de esteroides tan breve no suprime significativamente el eje hipotalámico-pituitario-adrenal. (17)
En caso de considerar una recaída severa y requerir hospitalización se recomienda plasmaféresis sobre las altas dosis de corticoesteroides.
En pacientes con EM que desarrollen una recaída y que estén infectados por COVID-19 los esteroides deben de ser evitados debido a que los mismos retrasan el aclaramiento de patógenos además de producir un estado de inmunosupresión. (18)