Introducción
El síndrome de encefalopatía posterior reversible (PRES), es un síndrome clínico-radiológico, de etiología muy variada, potencialmente reversible, caracterizado por una variedad de signos y síntomas neurológicos y hallazgos en neuroimagen compatibles con edema vasogénico(1)(2)(3).
Descrito por primera vez en 1996 por Hinchey, et al. en una serie de 15 pacientes que presentaron cefalea, alteración del estado mental, convulsiones, trastornos visuales y déficits neurológicos focales de rápido inicio, acompañados de lesiones en neuroimagen (en tomografía o resonancia magnética) compatibles con edema cerebral(1)(4)(5). A partir de esta descripción, se han reportado numerosos informes de casos y series de casos de PRES, en casi todos los grupos de edad, desde niños a adultos mayores, así como estudios observacionales retrospectivos; sin embargo no se han realizado estudios aleatorios, lo cual limita los datos epidemiológicos, criterios de diagnóstico y tratamiento(1).
La patogénesis del síndrome no se entiende completamente, siendo por lo general atribuida al incremento de la presión arterial media (PAM), que supera la capacidad de autorregulación cerebral, produciendo aumento de la presión capilar y permeabilidad de la barrera hemato-encefálica, con la consecuente extravasación de fluido en el parénquima cerebral, afectándose principalmente la circulación posterior por su menor inervación simpática. Esta teoría no explica gran cantidad de casos de PRES, ya que el 30% de los pacientes no presentan cifras de PAM elevadas en el momento de la presentación, y los pacientes tienen más edema en el territorio de circulación anterior que posterior; por lo que se postuló la teoría del daño endotelial ocasionado por un agente tóxico circulante que provoca vasoespasmo, hipoperfusión, isquemia con edema citotóxico posterior y activación de la cascada de coagulación; sin embargo no todos los pacientes con el síndrome tienen un agente tóxico conocido que interrumpa el endotelio, por lo que la fisiopatología del síndrome continua por dilucidarse(1)(4)(5)(6).
Presentamos a continuación, el caso de un paciente de 38 años de edad, con múltiples comorbilidades, quien presentó crisis convulsivas posterior a la transfusión de un concentrado de glóbulos rojos, asociado a lesiones compatibles en edema cerebral tanto en tomografía de cráneo como resonancia magnética.
Caso Clínico
Paciente de 38 años de edad, sexo masculino, con antecedentes de insuficiencia renal de causa no filiada desde los 16 años de edad, receptor de trasplante renal a los 20 años, recibiendo inmunosupresión a base de azatioprina y prednisona durante doce años. A los 32 años presenta elevación de azoados, por lo que se modifica tratamiento a micofenolato y prednisona, mantenido hasta la actualidad. A los 37 años se realiza biopsia renal, cuyo reporte es compatible con rechazo al trasplante, iniciando terapia biológica (Rituximab) con respuesta parcial. Es admitido en nuestra casa de salud por presentar deshidratación severa, síndrome diarreico agudo, insuficiencia renal crónica reagudizada de trasplante renal. Presenta además eritema, edema, calor en región inguinal derecha, con orificio de salida de material purulento de una semana de evolución.
El reporte de laboratorio informó: Leucocitos: 31160 Neutrófilos: 28920 Linfocitos: 620 Monocitos 1360 Hemoglobina: 9.9 gr/dl Hematocrito: 30.4% VCM: 77.2 HBCM: 2.1 Plaquetas: 468.000. PCR: 115, Procalcitonina: 1.34, Glucosa: 78, NA: 134, K: 5.8, CL: 106, Mg: 2.08, Ca: 8.6, P: 6.2, Urea: 113, Creatinina: 4.01 (MDRD: 17.9 ml/min/1.73m2), Bicarbonato: 13. Elemental y microscópico de orina: proteínas 150, sangre: 10. Proteínas séricas: 5.3, albúmina: 2.9, globulinas: 2.42. Se tomaron muestras para hemocultivos y cultivo de heces que reportaron negativos. El urocultivo reportó Klebsiella Pneumoniae productora de BLEE.
Ecografía abdomen inferior reveló colección paravesical derecha. El paciente recibió tratamiento a base de hidratación y antibioticoterapia (vancomicina, meropenem y metronidazol), además continuó con tratamiento inmunosupresor con micofenolato de mofetilo y prednisona.
A pesar del tratamiento, continúa debito purulento en región inguinal, por lo que realizan debridamiento de tejido desvitalizado con estudio de líquido purulento y ganglio abscedado de cadena inguinal derecha. Se recibió reporte de tuberculosis por ADN/PCR detectado con posterior inicio de tratamiento antifímico.
Tras restauración de volemia paciente presentó valores de Hb 6 g/dl en varios controles, sin evidencia de sangrado, por lo que decidieron transfusión de concentrados de glóbulos rojos, 2horas posteriores a la transfusión de 1 concentrado presentó convulsiones tónico clónicas generalizadas por 3 ocasiones. En ese momento paciente afebril, normotenso, normoglicémico. Examen neurológico posterior al evento relevó únicamente leve dismetría. Exámenes de laboratorio: Leucocitos: 15200 Neutrófilos: 12640 Linfocitos: 880 Monocitos 1410 Hemoglobina: 9.1 gr/dl Hematocrito: 27.1% Plaquetas: 531000, Procalcitonina: 3.67, NA: 132, K: 3.1, CL: 98, Mg: 5.2, Ca: 8.2, P: 5.2, Urea: 108.7, Creatinina: 3.35, Bicarbonato: 16, Elemental y microscópico de orina: proteínas 150, sangre: 10. Proteínas séricas: 5.3, albúmina: 2.9, globulinas: 2.42. TAC de cráneo: revela múltiples hipodensidades en parénquima cerebral. Resonancia magnética identifica varias lesiones hipointensas en T1, hiperintensas en T2 y aumento de la sensibilidad en FLAIR en parénquima cerebral y cereberal. En difusión se evidencia zonas con falta de restricción (Figura 1). Estudio de líquido cefaloraquídeo: Recuento leucocitario: 5 u/L, Hematíes: 2000 u/L, polimorfonucreares: 80% mononucleares: 20%, glucosa 65 mg/dl, proteínas: 40.7 mg/dl, LDH 17 u/L, lactato: 1.8. GRAM, cultivo de LCR, tinta china y tinción de Ziehl-Neelsen: negativo. Tuberculosis por ADN/PCR: no detectado. Electroencefalograma: infrecuentes descargas punta onda generalizada de 3Hz/s.
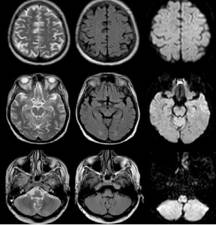
Nuestro paciente recibió tratamiento anticonvulsivante con levetiracetam. No presentó nuevos episodios de convulsión ni alteraciones al examen neurológico. Resonancia magnética realizada 16 días después revela regresión de las lesiones previas (Figura 2).
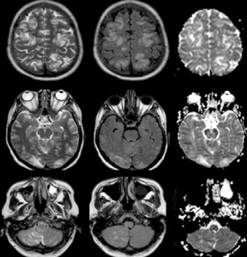
Figura 1 Secuencias T2, T2 FLAIR y DWI Sense en Resonancia magnética realizada el día de presentación de convulsiones, se evidencian múltiples lesiones en parénquima cerebral y cerebelosa.
Discusión
Son múltiples las causas asociadas a PRES como: hipertensión arterial severa, insuficiencia renal, infección severa, sepsis, fármacos citotóxicos, enfermedades autoinmunes sistémicas, preeclampsia o eclampsia, trasplantes de órganos sólidos o de médula ósea, terapia inmunosupresora, quimioterapia, púrpura trombocitopénica trombótica, alteraciones hidroelectrolíticas como hipomagnesemia, exposición a medios de contraste, fármacos como ivabradina, eritropoyetina, entre otras(3)(4).
En una cohorte de 4222 pacientes que se sometieron a trasplante de órgano sólido entre 1998 a 2006, la incidencia general de PRES fue del 0,49%, con una incidencia del 0,34% en los pacientes del grupo de trasplante renal o riñón-páncreas(7). Un análisis de literatura desarrollado por Song, et al, determinó el tiempo medio de aparición después del trasplante de órganos en 17 días (rango: 24 horas a 5 años), con un 7.3% de aparición después del primer año del trasplante.
Los inhibidores de la calcineurina, usados como agentes inmunosupresores primarios se atribuyen a la neurotoxicidad en 20% a 40% de estos pacientes(8), y su asociación se encuentra reportada en varios de los casos publicados de PRES en pacientes postrasplante renal(8)(9)(10). En reportes de casos la inmunosupresión con micofenolato se ha asociado con enfermedades sistémicas como lupus eritematosos sistémico(11)(12).
La relación de PRES con infección grave o sepsis a menudo está asociada con bacterias gram-positivas, por lo general en pacientes que reciben inmunosupresión y presentan fallo renal agudo(4).
En el caso de nuestro paciente podemos encontrar posible asociación en el contexto de un paciente postrasplante renal, con insuficiencia del riñón trasplantado, séptico, quien recibió terapia inmunosupresora por 18 años; sin embargo, el síndrome se presentó inmediatamente posterior a la transfusión de un concentrado de glóbulos rojos en un paciente con anemia crónica, reportándose una elevación de 3 g/dl de hemoglobina.
Hasta el año 2018, en la literatura se reportan únicamente 21 casos de PRES posterior a la transfusión de sangre ocasionados por la corrección rápida de la hemoglobina (Tabla 1). 15 casos fueron reportados en el contexto de anemia crónica, la mayoría fueron mujeres de edad media, 3 casos, como el nuestro, asociaron la falla renal a la causa de anemia y las convulsiones fueron la principal manifestación clínica reportada (13)(14)(15)(16)(17)(18)(19)(20)(21)(22)(23)(24)(25)(26)(27)(28)(29).
Se considera que la anemia crónica crea un ambiente de estrés hipóxico que ocasiona vasodilatación cerebral. La corrección rápida de la anemia reduce esta señalización produciendo rápida vasoconstricción predominantemente en regiones occipital y temporal del cerebro, lo cual lleva a la liberación de citoquinas inflamatorias que lesionan el endotelio y conducen al aumento de la permeabilidad vascular. La PCR elevada e hipoalbuminemia promueven la disfunción endotelial(13).
La resonancia magnética nuclear es el método de elección, ya que permite diferenciar PRES de lesiones isquémicas agudas. Las imágenes muestran comúnmente edema vasogénico que afecta, casi simétricamente, a las regiones subcorticales de los lóbulos occipital, temporal posterior y parietal(3)(4). En un estudio observacional, retrospectivo realizado en un hospital de la India, que incluyó 24 pacientes ingresados en el servicio de neurología entre 2014 y 2017, de los 62.5% a quienes se realizó TAC de cráneo el 80% presentaban imagen normal. La resonancia magnética mostró afectación parietooccipital en 62.5%, 33% tuvo afectación difusa cerebral y en el 16.6% de pacientes se observó participación de ganglios basales y cerebelo(2).
En el caso de nuestro paciente la TAC de cráneo simple revelo varias imágenes hipodensas difusas en parénquima cerebral, hallazgos que se relacionaron con las imágenes de RM, además de lesiones cerebelares reflejadas en la RM.
El diagnostico diferencial imagenológico incluye patologías como la gliomatosis cerebral y otros tumores cerebrales, encefalitis de etiología infecciosa (bacteriana, viral, parasitaria o fúngica), o inmunomediada (Encefalitis autoinmune mediada por NMDA, AMPA, etc.), manifestaciones neurológicas primarias o secundarias asociadas a la infección por el virus de inmunodeficiencia humana VIH exposición a tóxicos ambientales (monóxido de carbono y metales pesados), entre las patologías más comunes que deben ser descartadas mediante protocolos de investigación adecuados.
El manejo de PRES es sintomático, con especial control en tensión arterial para evitar complicaciones como infarto, hemorragia cerebral, herniación del cerebelo, estado epiléptico refractario y epilepsia a largo plazo(1)(5).
El pronóstico de esta afección es favorable, con una resolución completa en el 84% de los casos y mortalidad menor al 6%, la mayoría de pacientes alcanzan su recuperación clínica completa en pocos días, con desaparición de lesiones en imágenes en semanas o meses(1)(4).
En nuestro paciente pudimos evidenciar la resolución completa de los síntomas y casi resolución de las lesiones por imagenen el control de resonancia magnética realizado a los 16 días del evento.
Conclusión
En general, PRES es una patología benigna, que se presenta en una gran variedad de contextos clínicos. La importancia de nuestro reporte radica en el pequeño número de casos que se encuentran en la literatura asociados a transfusión de glóbulos rojos, ya que si bien nuestro paciente presenta múltiples patologías que han sido descritas como factores etiológicos de PRES, estas se habían instaurado ya previamente sin producir afectación encefálica y fue solo tras transfusión de glóbulos rojos y la subida rápida de 3.1 g/dl de hemoglobina que se presentó el síndrome.
Los hallazgos clínicos y los cambios imagenológicos en resonancia magnética nos permiten poner sobre la mesa el diagnostico de PRES, para de esa forma brindar mejores oportunidades diagnosticas y terapéuticas en presencia de casos multifactoriales como el previamente descrito.