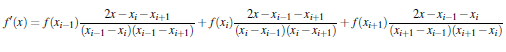Forma sugerida de citar:
Bautista, G., Mátyás, B., Singla, A., Serrano, V., Morales Arteaga, J., Sánchez, R. G., bracho Velásquez, R. D. and Ramírez-Cando, J. L.. 2018. Variaciones altitudinales en iones de H y Al en el contenido de Fe en suelos de la selva amazónica. La Granja: Revista de Ciencias de la Vida. Vol. 28(2):43-51.http://doi.org/10.17163/lgr.n28.2018.03.
1 Introducción
El estudio de los suelos requiere un enfoque interdisciplinario que involucre a geólogos, físicos, químicos,biólogos, entre otros (Brevik et al., 2015). Sinembargo, no existe la suficiente atención a pesar que son precisamente los suelos el medio de cultivo para la alimentación, y sus propiedades se consideran indicadores de numerosos procesos naturales y artificiales (Coyago y Bonilla, 2016; Ulloa et al., 2014; Yánez y Bárcenas, 2012) y de la biodiversidad (Guevara et al., 2018); como consecuencia, en la actualidad no hay suficientes investigaciones que se enfoquen en el suelo como base para la alimentación. Por lo tanto, las investigaciones llevadas a cabo para analizar los efectos del manejo orgánico del suelo versus el manejo convencional son cada vez más importantes para la agricultura sostenible (Bautista et al., 2017; Mátyás, Andrade, Chida, Velasco, Morales, Montero, Cando y Acevedo, 2018; Taipe Velasco,Lizano Acevedo y Mátyás, 2018). Cabe señalar que en Ecuador se ha venido estudiando el suelo gracias a otra área de investigación como es la Astrobiología, que es la investigación que busca evidencias de moléculas relacionadas con la vida o rastros de una vida anterior en planetas remotos, y que es cada vez más importante en el país debido a sus características naturales que permiten analizar los suelos analógicos extraterrestres (Mátyás, Bautista, Szarka, Serrano, Arteaga, Loja, Yaguana, Gómez y Ramírez-Cando, 2018).
Ambas áreas de investigación requieren un análisis de suelos sin cultivos como muestras de control, especialmente la Astrobiología, ya que las muestras que tienen una actividad microbiana significativa, como en la selva amazónica, pueden ser consideradas confiables (Mátyás, Bautista, Szarka,Serrano, Arteaga, Loja, Yaguana, Gómez y Ramírez-Cando, 2018). Los suelos varían ampliamente en la Amazonía con una gran diversidad, características morfológicas y propiedades físico-químicas del suelo (Quesada et al., 2010). Las investigaciones de las propiedades del suelo en estas áreas ayudan a obtener un conocimiento general de los suelos nativos einexplorados (Quesada et al., 2011). También, en la literatura existen importantes investigaciones que examinan los bosques amazónicos en un ambiente heterogéneo en relación con el suelo y la topografía (de Castilho et al., 2006).
La acidificación del suelo es un proceso natural condicionado por rocas de origen natural ácido, altas precipitaciones y lenta descomposición de materia orgánica, produciendo diversos ácidos orgánicos (Pavlu et al., 2007). La existencia de una alta acidez cambiable en el suelo generalmente indicala ocurrencia del hidrógeno cambiable (H), aluminio cambiable (al), ion libre de AL3+ o compuestos Al-hidróxidos parcialmente neutralizados (Hinrich, Brian y O’Connor George, 2001). También se ha observado que la mayor parte del carbono estable en subsuelos ácidos está asociado con hidróxidos poliméricos de Fe y de Al, ferrihidrita, y con óxidos de Fe cristalinos (Mikutta et al., 2006; Spielvogel, Prietzely Kögel-Knabner, 2008).
Por lo anteriormente expuesto, se recolectaron muestras de suelo de 3 profundidades y de 9 alturas diferentes en la selva amazónica. Así, el presente estudio proporcionará los efectos de la profundidaddel suelo y de las variaciones altitudinales en el contenido de Fe y el intercambio de iones H-Al. Además, se detectaron moléculas orgánicas en una de las muestras recolectadas, proporcionando valores de control para fines de investigación astrobiológica.
2 Métodos
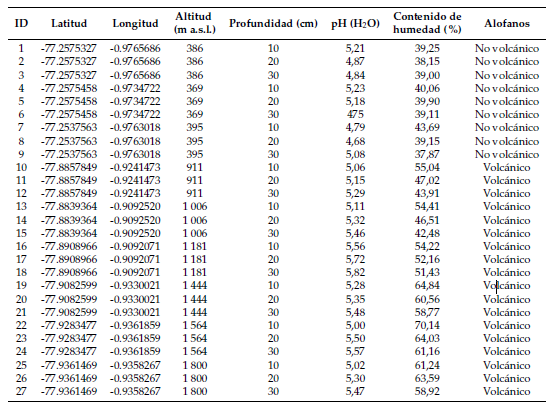
Se colectaron un total de 27 muestras de suelo cerca de Tena (selva amazónica), Ecuador, el 15 de mayo de 2018, desde la capa superior a nueve altitudes diferentes del suelo tipo Hyperalic Alisol (Tabla1). Se midió el pH en agua destilada y en 1m de NAF (suelo/agua, 1/2,5, w/w) de acuerdo a lo propuesto por Buzás (1988). El contenido de humedad del suelo se midió gravimétricamente, secándose a 105°C durante 24 horas según el método Díaz-Romeu y Hunter (1982). Se detectó alofano (Tabla 1) según el método Fieldes (1986) usando 10g suelo/agua (1:2), suelo/agua +20ml 1M NAF, suelo/agua (1:2,5) +25ml 1M NAF, suelo/agua (1:2,5)+25ml 0,5 M NAF como se describe a continuación. Para la preparación de la muestra se agregaron 20ml de agua destilada a 10g de muestra de suelo y se midió el pH, luego se agregaron 20ml de fluoruro sódico (1M) a la solución y se midió de nuevo el PH. Adicionalmente, se agregaron 25ml de agua destilada a 10g de muestra y se midió de nuevo el pH. Se agregaron 25ml del fluoruro del sodio (el 1M) ala solución y finalmente se midió de nuevo el pH. Cuando el pH es mayor a 9 durante la medición sugiere que el alofano está presente debido al origen volcánico de la muestra (Tabla 1).
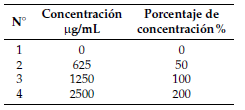
El contenido de Fe se midió según el método modificado de (Blakemore, 1981) de la siguiente manera: para preparar las muestras se agregaron 50ml de oxalato amónico monohidrato (0,2 M, pH= 3) a 1g de la muestra del suelo. La mezcla se revolvió durante 4,5 horas en 150 RPMs (usando NB-101M, N-Biotek Inc, Corea). La mezcla se centrifugó a 15 min a 3500 RPM (usando Hermle Z400, Hermle AG, Alemania) para obtener el sobrenadante 12 horas después. A continuación se realizó un doble proceso de filtrado con el papel de filtro de No. 42. Para determinar la concentración de la curva de calibración (Tabla 2) se utilizó como disolvente la solución de extracción de ácido de amonio oxalato (0,2 m). Se adicionaron 2,5 g de metal de hierro en 35 mL de ácido clorhídrico 1:1 y se diluyó en 1,5 L añadiendo 2500 g/ml de Fe. Finalmente, la solución se midió usando un espectrofotómetro de absorción atómica (longitud de onda: 392 nm; anchura de la hendidura: 0,2 nanómetro).
La acidez intercambiable se determinó según elmétodo modificado de Salinas y García (1979) citado en Coleman y Thomas (1967); Lin y Coleman (1960); Pratt y Bair (1961) utilizando 10 ml de extracto obtenido con 1N KCl, 10 ml de agua destilada, 0,05% fenolftaleína y 0,01 n NaOH de la siguiente forma: para preparar las muestras se añadieron 25 ml de cloruro de potasio (1N) a 2,5 g de la muestrade suelo. Luego se agitó (usando NB-101M, NBiotekInc, Corea) por 15 minutos en 60 rpm. Parafiltrar la solución se usó un papel filtrante No. 42.Se agregaron 10 ml de agua destilada a 10 ml del filtrado. Luego, se adicionaron aproximadamente tres gotas de 0,05% fenolftaleína, y la solución se tituló por 0,01 n NaOH. Se usó la siguiente fórmula para calcular los resultados:
Acidezintercambiable(mEq=100gdesuelo) =CantidaddeNaOH NNaOH (100=pesodelamuestradesuelo)
En donde:
La acidez intercambiable se (expresa en mEq/100gsuelo),
La cantidad de NaOH es la pérdida de NaOH durantela titulación (expresada en mL), N NaOH es la concentración de NaOH usada parala titulación (expresada en N),
El peso de la muestra del suelo es el peso de la muestra usada para las mediciones (expresada eng).
Se detectaron compuestos orgánicos en la muestra seca y fresca del suelo (ID = 10) vía HPLC (agua 1525 bomba binaria HPLC con detector de diodo de aguas 2998); espectrofotometría (espectrofotómetro Jasco V-730 y Perkin Elmer Spectrum BX) y GC/MS(EVOQ Scion 436-GC, Bruker). El SDS-VAGE se realizó según Warrant el al. (2003) en el sistema vertical de gel de Enduro ES. Los resultados obtenidos de la cromatografía se combinaron con Wiley NIST2014-XI edición GC/MS. Se aceptaron identificaciones de compuestos orgánicos cuando la probabilidad del criterio de similitud fue P>0,9 (Mátyás, Bautista,Szarka, Serrano, Arteaga, Loja, Yaguana, Gómezy Ramírez-Cando, 2018).
Se aplicó el modelo ANOVA para el análisis estadístico, a fin de verificar si existen diferencias en las altitudes y profundidades en los parámetros examinados. Se utilizó la prueba de Duncan como análisis post hoc. Para ilustrar los resultados de la concentración y de la absorbencia del Fe (ABS) en las diferentes altitudes se aplicó la fórmula de interpolación de Lagrange para la primera derivada, que resulta adecuada para examinar datos desigualmente espaciados:
En donde:
x Es la altitud en donde se calcula el primero derivado,
xi−1 ; xi ; xi+1 son las altitudes determinadas (El orden no es relevante),
f (xi−1); f (xi); f (xi+1) son las concentraciones de Fe relacionadas a las altitudes, respectivamente.
Nota: consulte el apéndice para ver el código de Visual Basic para aplicaciones (VBA).
También se aplicó un modelo de almacenamientode datos no relacional JT (Mátyás, Bautista,Szarka, Serrano, Arteaga, Loja, Yaguana, Gómezy Ramírez-Cando, 2018; Mátyás et al., 2016a, b) en un servidor Oracle Application Express (ORACLE,N.d.), para almacenar los datos que no han sido experimentadosy los resultados evaluados.
3 Resultado
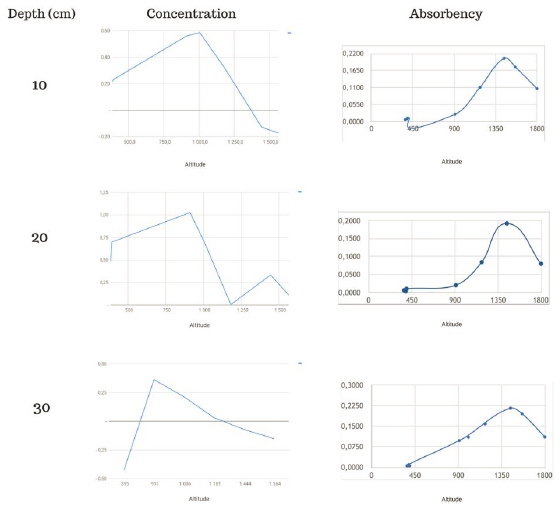
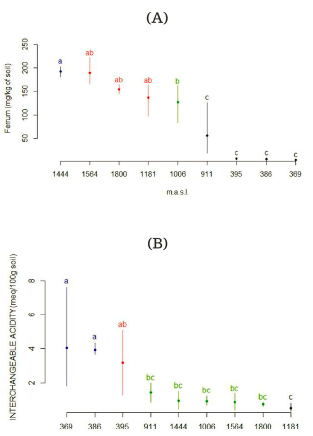
La Figura 1 corresponde a la primera derivadadel contenido de Fe (concentración y absorbencia) en las altitudes estudiadas. Se observa un patrón bastante linear en las profundidades (especialmente a 10 centímetros). En las tres gráficas se evidencia que los valores de los derivados alrededor de 1 000 y 1 200 msnm son negativos o similares. Se observó la concentración más alta de Fe, 222 mg/kg en 1 564 msnm a una profundidad de 20cm; mientras que la concentración más baja de Fe,2,27 mg/kg se midió en 386 msnm a una profundidad de 20 cm. Se observa una clara tendencia decreciente en los valores de concentración a medida que disminuye la altitud.
Los gráficos ABS de las diferentes profundidades son bastante similares y lineales. Se puede observar el punto de entrada alrededor de 1444msnm, donde la pendiente de la curva se vuelve negativa. El comportamiento en las tres curvas entre 400 y 1000 msnm es bastante similar en las dos primeras gráficas; siendo bastante liso y con una curva ascendente (hasta 1444 m msnm). En el tercer gráfico (correspondiente a una profundidad de 30 cm) se evidencia una sección bastante lineal con una curvatura casi imperceptible.
Los resultados estadísticos demuestran que no existem diferencias significativas en la concentración de Fe y la acidez intercambiable en las diferentes profundidades (p=0.85). Por otro lado, se pueden observar fuertes diferencias aplicando ANOVA en las altitudes (p =0,00005). En la Figura 2 la prueb aDuncan resume a los grupos para los parámetros evaluados con respecto a las diferentes altitudes. Esta información presenta las medias y los intervalos de confianza para cualquier altitud en los ensayos. Los valores de concentración de Fe disminuyen a medida que reduce la altitud (Figura 1. A).
Se detectaron alcoholes de azúcares, ácidos hidróxidos y oxoácidos usando HPLC. De igual forma, se encontró carbono (48,1%), nitrógeno (7,6%) y aminoácidos (7,9%) mediante electroforesis. Se detectó glicerol, ácido oxálico, ácido masónico, ácido glutárico, ácido glicólico, ácido 4-hydroxybenzonicy ácido 3,4-dihydroxybenzonic por GC/MS (Mátyás, Bautista, Szarka, Serrano, Arteaga, Loja, Yaguana,Gómez y Ramírez-Cando, 2018)).
4 Conclusiones
Se concluyó que la profundidad del suelo no afectó significativamente el contenido de Fe y la acidez intercambiable; mientras que la altitud afectó a ambos. El presente estudio indicó que la altitud, en comparación con la profundidad del suelo, puede desempeñar un papel importante en el contenido de Fe y la acidez intercambiable. Además, la alta cantidad de moléculas orgánicas que podrían ser detectadas por instrumentos analíticos sugieren que los sitios de muestreo seleccionados pueden proporcionar muestras prometedoras para evaluar suelos analógicos extraterrestres para futuros análisis.