1. Introducción
En el Ecuador existen comunidades que dependen del agua superficial no tratada como su fuente primaria de agua potable (Rao et al., 2015). Lamentablemente, estas fuentes superficiales son el sumidero de aguas servidas que contienen residuos humanos con una gran carga bacteriana, en especial de coliformes fecales.
La ingestión de agua contaminada representa uno de los principales causantes de enfermedades gastrointestinales en humanos y se ha descrito que en los países en desarrollo E. coli causa el 40% de las diarreas en niños menores de 5 años (OMS, 2015; Levy et al., 2012). Se calcula que anualmente mueren 2.5 millones de niños por diarreas a nivel mundial (OMS, 2013). En el Noreste de Ecuador la prevalencia de E. coli es de 8 personas infectadas por cada mil personas (Bhavnani et al., 2016).
En la búsqueda del origen de la contaminación por E. coli en Ecuador, algunos autores han estudiado el agua de varios ríos donde se determinaron altas concentraciones de coliformes totales y fecales. En la provincia de Esmeraldas, se ha reportado la presencia de E. coli en los ríos Onzole (1248 NMP/100 ml), Cayapas (474 NMP/100 ml) y Santiago (2420 NMP /100 ml) (Wafaa et al., 2007). De igual forma, en la provincia del Guayas, en el río Yaguachi encontraron concentraciones de E. coli de 5214 NMP/100 ml (Valencia, 2018) y en la provincia de Pichincha, en el río Quevedo 126000 NMP/100 ml (Robinson, 2015) valores superiores a los límites máximos permisibles, lo que indica que el agua de estos ríos no es apta para consumo humano, riego agrícola ni para uso pecuario. La causa de esta contaminación es el vertido a los ríos de aguas servidas sin previo tratamiento.
El efecto de la contaminación del agua se refleja en los altos niveles de parasitosis, enfermedades diarreicas, y pérdida de la biodiversidad acuática relacionadas con la mala calidad del agua en el Ecuador (Universidad Agraria del Ecuador, 2009). Según la Dirección Nacional de Vigilancia Epidemiológica del Ministerio de Salud Pública de Ecuador, en el año 2016 en la provincia de Guayas, por cada 100000 habitantes se presentaron los siguientes casos de infecciones gastrointestinales: 3033 casos de enfermedades diarreicas, 1206 de Shigelosis, 90 de Síndrome Diarreico Agudo con deshidratación y 9 de Salmonelosis (Dirección Nacional de Vigilancia Epidemiológica, 2017).
Dentro de los tratamientos que se han propuesto para saneamiento de las aguas residuales se encuentran la cloración, el tratamiento de lagunaje facultativo y la fotocatálisis heterogénea. La eficiencia de remoción de coliformes de los tratamientos tradiciones se encuentran en rangos de 55,6% con cloración, 90% con tratamiento de lagunaje facultativo y 100% utilizando fotocatálisis heterogénea con TiO2 (Rojas-Higuera et al., 2010). Sin embargo, estos tratamientos son costosos y poco asequibles para la población rural. Actualmente se están probando nuevas técnicas que son más económicas y amigables con el ambiente. Una de estas técnicas es la fitorremediación, en la cual se utilizan plantas para remover, detoxificar y contener contaminantes orgánicos e inorgánicos del agua (Castrillo et al., 2012; Gerhardt et al., 2017; Wang et al., 2017). En estudios previos se observó que los coliformes fecales pueden ser removidos en un 99% por las especies E. crassipes (Vizcaino et al., 2016), L. minor (Valderrama et al., 1987) y Phragmites australis (Mantovi, 2003).
Varios mecanismos físicos, químicos y biológicos para la remoción de coliformes fecales y bacterias patógenas en sistemas de fitorremediación han sido descritos (Wu et al., 2016). Entre los mecanismos físicos se encuentran la filtración mecánica, sedimentación y la adsorción a materia orgánica. Dentro de los biológicos la muerte natural (Green et al., 1997) y la retención en biopelículas (Brix, 1997) y los mecanismos químicos incluyen oxidación y exposición de biocidas excretados por las plantas (Axelrood et al., 1996).
Las especies más utilizadas para la fitorremediación de aguas contaminadas son plantas acuáticas ya que poseen la habilidad de absorber, eliminar o neutralizar compuestos inorgánicos y orgánicos (Delgadillo y González, 2011). En Ecuador se desconoce la capacidad de las plantas acuáticas para remover coliformes fecales y E. coli y por ello, el objetivo del presente trabajo fue determinar el potencial de plantas acuáticas para remover coliformes totales y E. coli en aguas servidas.
2. Metodología
Áreas de Estudio
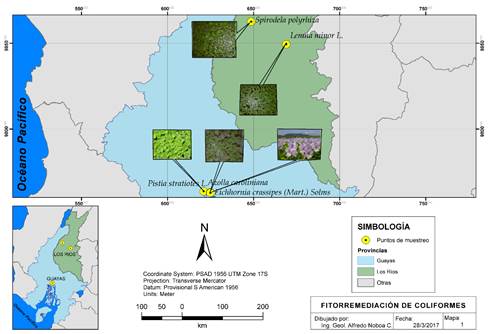
Se recolectaron las especies Eichhornia crassipes (Mart.) Solms, Azolla caroliniana Willd y Pistia stratiotes L. en el río Guayas, provincia de Guayas, Ecuador (Figura 1). El helecho acuático Salvinia auriculata Aubl. y la planta Spirodela intermedia W. D. J. Koch se colectaron en el estero Peñafiel, recinto Jauneche, provincia de Los Ríos. En el recinto Aguas Frías, provincia de Los Ríos se obtuvo Lemna minor L. y Ceratopteris thalictroides (L.) Brongn fue adquirida en Acuario Kattu, Alborada, provincia de Guayas, Ecuador.
La especie Lemna minor se ha descrito como una planta acuática capaz de remover 98-99% de coliformes totales en aguas servidas (Valderrama et al., 1987) y por ese motivo se seleccionó como control positivo.
Muestras de aguas servidas
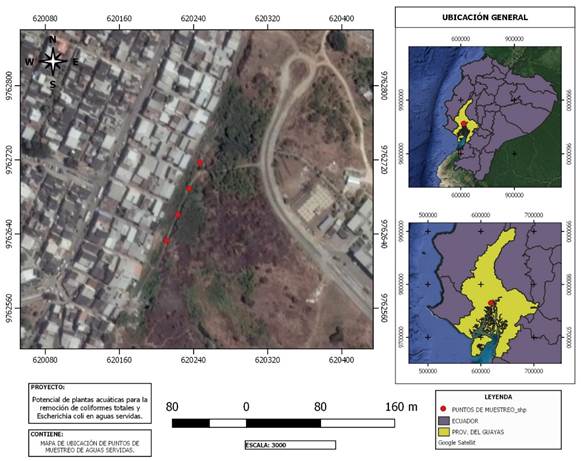
Se establecieron 4 puntos de muestreo a lo largo de la zanja de aguas servidas ubicada dentro del Campus Mapasingue de la Universidad de Guayaquil, provincia de Guayas. Para ello se realizó un transecto donde se tomaron cuatro muestras a 30 m de distancia entre ellas, para un total de 4 muestras (Figura 2).
Para colecta de las muestras de aguas servidas se utilizaron recipientes estériles de 20 L de capacidad y se sumergieron en el centro de la zanja, luego fueron secados y desinfectado su exterior con alcohol al 70%, posteriormente las aguas de los envases fueron vaciadas en un contenedor con la finalidad de homogenizar la muestra, por un lapso de 4 h previo a su uso para el ensayo.
Reproducción de las plantas
Las especies colectadas en el campo se reprodujeron bajo condiciones naturales. Para ello, las plantas se colocaron en envases de plástico transparentes con 3 L de agua y fertilizante Multiflor® según las indicaciones del fabricante a 25º-30ºC y luz natural (2000 lux).
Reproducción de E. coli ATCC 25922
Se reactivó la cepa E. coli ATCC 25922 en 5 ml de agua de Peptona (Merck), posteriormente se sembró 200 µl en una placa de agar Chromocult (Merck) a temperatura de 35-37°C durante 18-24 h. Se tomaron 2-3 colonias para realizar un inóculo bacteriano en 5 ml de solución salina 0.9% y de él se adicionó 1 ml a 30 ml de agua de peptona por un lapso de 18-24 h.
Reproducción de coliformes totales
Los coliformes totales se aislaron de las muestras de aguas servidas. Se tomó 1 ml del agua servida y se sembró en medio agar Chromocult (Merck) a temperatura de 35-37°C durante 18-24 h y se verificó que no hubiese E. coli. Posteriormente, se aislaron en agar Chromocult y luego se purificaron en agar TSA (Merck).
Capacidad de las plantas para remover E. coli ATCC 25922 y coliformes totales
Las plantas se aclimataron durante 7 días previos al bioensayo. Al momento del ensayo las macrófitas se lavaron con agua corriente, destilada y se colocaron 4 g en envases de plástico. Posteriormente, se realizaron los ensayos en vasos de precipitación de 500 ml por triplicado a las cuales se inoculó una cepa de referencia E. coli ATCC25922 y coliformes totales con una concentración que se determinó previamente en cada ensayo y con un tiempo de retención de 7 días, después de ese lapso se determinó la carga bacteriana remanente. Estos ensayos se realizaron a 25°C y luz artificial fluorescente de 800 lux con un fotoperíodo de 12 horas.
El control negativo empleado estaba formado por la bacteria E. coli y coliformes Totales en agua destilada sin plantas y un control positivo con L. minor. A los 0 y 7 días de retención se determinó la concentración de E. coli y coliformes totales y los porcentajes de remoción según la metodología descrita en el apartado de parámetros bacteriológicos, así como los parámetros fisicoquímicos temperatura, pH y sólidos suspendidos según las técnicas estandarizadas (APHA/AWWA/WEF, 2012).
Capacidad de las plantas para remover E. coli y coliformes totales de aguas servidas
Una vez obtenida el agua servida, se determinó la presencia de coliformes totales y E. coli utilizando el medio de cultivo Agar Chromocult (Merck®) según la técnica EPA1.10426. El ensayo se desarrolló en recipientes con capacidad de 1000 ml y se utilizaron 500 ml de aguas servidas en cada envase con un tiempo de retención de 7 días. Para determinar la concentración de las bacterias se realizó un cultivo con la técnica de vertido en placa para contaje de unidades formadoras de colonias (UFC). A los 7 días de retención se determinó la concentración de E. coli y coliformes totales y los porcentajes de remoción según la metodología descrita en el apartado de parámetros bacteriológicos, así como los parámetros fisicoquímicos temperatura, pH y sólidos totales disueltos (TSD) según las técnicas estandarizadas (APHA/AWWA/WEF, 2012).
Parámetros bacteriológicos
Para los análisis se utilizó el medio de cultivo selectivo agar Chromocult, aprobado por la EPA y la AOAC para la detección simultánea de coliformes totales y E. coli en muestras de agua. Se utilizó el método vertido en placa, tanto para las muestras inoculadas con E. coli y las muestras de aguas servidas. Se tomó 1 ml de la muestra de agua proveniente de cada ensayo a las cuales se realizó diluciones sucesivas de 10-1, 10-2,10-3, 10-4 y 10-5 en medio peptona, se tomó 1 ml de cada dilución y se sembró en cajas Petri, luego se agregaron 18 ml de agar Chromocult, se homegenizó y dejó solidificar por 10 min. Posteriormente, se incubaron las placas a 37°C por 24 h y se procedió a contar las unidades formadoras de colonia. Para confirmar la presencia de E. coli se les agregó una gota de reactivo de Indol Kovacs, el mismo que dio una reacción positiva por el cambio de color rojo cereza después de unos segundos. Adicionalmente, se realizaron pruebas de tinción de Gram (Gram, 1884), oxidasa y motilidad (Montoya, 2008).
Análisis Estadísticos
Todos los resultados se muestran como promedio ± desviación estándar de n=3 muestras. Los gráficos se realizaron utilizando el programa Origin Pro 8.
Para realizar la comparación entre tratamientos se utilizó la prueba de normalidad de Anderson-Darling y un test de igualdad de varianza de Levene. Para las muestras con distribución normal se aplicó una prueba de Anova de una vía con test a posteriori de Tukey (p<0.05). Para las muestras que no presentaron distribución normal se aplicó una prueba no paramétrica de Kruskall-Wallis.
Finalmente, para verificar la relación entre los parámetros fisicoquímicos y la remoción de coliformes totales y E. coli se realizó un análisis de correlación de Spearman Rho. Para realizar todas las pruebas se utilizó el programa Minitab versión 17.
3. Resultados
Plantas seleccionadas
Las plantas seleccionadas fueron Spirodela intermedia W. D. J. Koch, Salvinia auriculata Aubl., Pistia stratiotes L., Eichhornia crassipes (Mart.) Solms, Ceratopteris thalictroides (L.) Brongn., Azolla caroliniana Willd y Lemna minor L. como control positivo.
Capacidad de las plantas para remover E. coli ATCC 25922 y coliformes totales
Una vez que las plantas fueron reproducidas se realizaron ensayos de laboratorio para verificar su capacidad de eliminar E. coli ATCC 25922 y coliformes fecales. Las especies S. intermedia, S. auriculata, P. stratiotes, E. crassipes y C. thalictroides, eliminaron en un 100% a las E. coli (Figura 3). Además, A. caroliniana, y L. minor redujeron en un 99% la población de E. coli en comparación al control 1.5×109/100 mL UFC. A. caroliniana redujo significativamente la concentración de 1.05×103/100 ml UFC a 7.07×101/100 ml UFC de E. coli y L. minor de 1.8×103/100 ml UFC a 8×102/100 ml UFC (H = 7.20; p = 0.027).
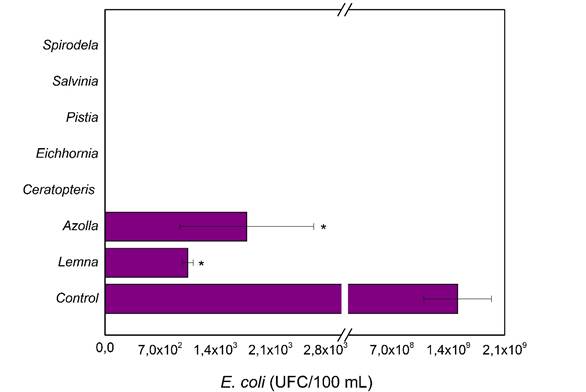
Fig. 3: Efecto del bioensayo con diferentes especies de plantas sobre la concentración de E. coli. Los resultados se muestran como medias ± desviación estándar. * Indica que existen diferencias significativas en comparación con el control según Kruskall-Wallis (p<0,05).
En cuanto a los coliformes totales (Figura 4), se encontró que E. crassipes obtuvo la menor tasa de eliminación de coliformes totales en comparación a las otras especies vegetales que eliminaron en un 100 % al agente bacteriano, pero hubo una reducción significativa de 7933 UFC/100 ml en comparación al blanco 1.29x107 UFC/100 ml (F = 41.58; p = 0.003).
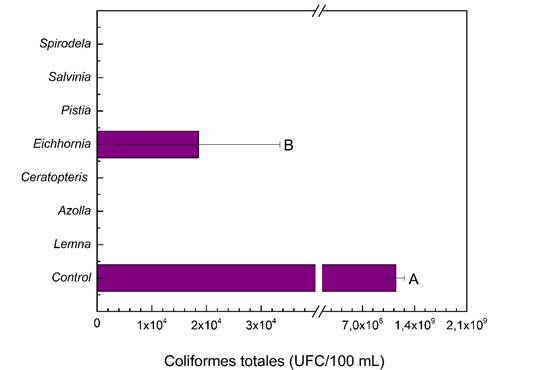
Fig. 4: Efecto del bioensayo con diferentes especies de plantas sobre la concentración de coliformes totales. Los resultados se muestran como medias ± desviación estándar. * Indica que existen diferencias significativas en comparación con el control según Anova de una vía y test a posteriori de Tukey (p<0,05).
Efectos sobre los parámetros fisicoquímicos
En el parámetro de sólidos totales disueltos (TSD), no se apreciaron diferencias significativas para la mayoría de las plantas (Tabla 1). C. thalictroides generó los niveles más altos de sólidos disueltos inclusive mayores a los del blanco, pero sus diferencias no son significativas según Kruskall-Wallis (p < 0.05). En contraposición la E. crassipes presentó los niveles más bajos de TSD de 62 mg/L (F = 6.82; p = 0.001).
Tabla 1 Efecto del bioensayo con diferentes especies de plantas sobre el pH, temperatura (T°C) y sólidos totales disueltos (TSD). Los resultados se muestran como medias ± desviación estándar.

* Indica que existen diferencias significativas en comparación con el control según Kruskall-Wallis (p<0,05)
Los parámetros de pH y temperatura a lo largo del ensayo se mantuvieron con una relativa estabilidad solo mediante el test de Kruskall-Wallis se encontró que poseen diferencias significativas. Las especies E. crassipes y S. intermedia presentaron un pH de 7,067±0,643 y 7,200±0,000, menor al control 8,067±0,058 (H = 18,99; p = 0.008).
Asimismo, la temperatura del agua se redujo significativamente para la mayoría de las especies para el día 7 del ensayo. En la Tabla 1 podemos observar que C. thalictroides, E. crassipes, P. stratiotes y S. auriculata presentaron un valor de 24,00±0,00 °C significativamente menor al control (26,33±0,57°C).
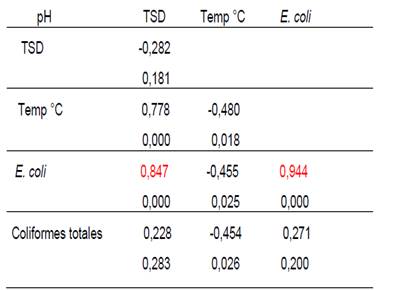
Se realizó una prueba estadística de Spearman Rho para evidenciar la relación entre los parámetros fisicoquímicos y la remoción de E. coli y coliformes totales, donde podemos apreciar en el Tabla 2, una correlación directa entre la concentración de E. coli y el pH (rs = 0,847; p = 0.000) y la temperatura (rs = 0,944; p = 0,000) lo que indica que a mayor pH y temperatura mayor concentración de bacterias.
Tabla 2 Análisis de correlación de Spearman entre los parámetros del bioensayo pH, temperatura, sólidos totales disueltos (TSD), concentración de coliformes totales y E. coli.
Contenido de Celdas: Spearman rho
P-Valor
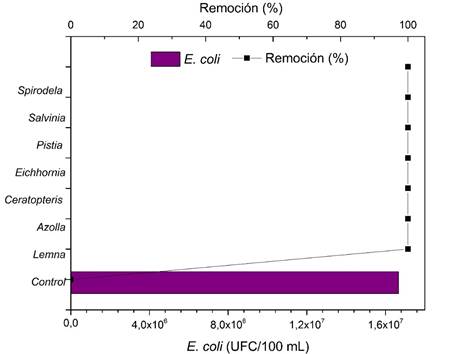
Figura 5 Efecto del bioensayo con diferentes especies de plantas sobre la concentración de E. coli en las aguas servidas. ▪ Indica el porcentaje de eficiencia de cada planta en la eliminación de E. coli.
Capacidad de las plantas para remover E. coli y coliformes totales de aguas servidas
Las plantas que mostraron una elevada tasa de eliminación tanto de coliformes como de E. coli se sometieron a un ensayo con aguas servidas para determinar la tasa de remoción. Las especies S. intermedia, S. auriculata, P. stratiotes, E. crassipes, C. thalictroides, A. caroliniana y L. minor alcanzaron una remoción del 99.97 % de E.coli en contraste con el control que inició con un contaje de 120 UFC/100 ml de E.coli y después de 7 días se elevó hasta 1.67x107 UFC/100 ml (Figura 5).
Así también, las plantas que mostraron una buena tasa de eliminación de coliformes totales con 100% de remoción fueron: S. auriculata y A. caroliniana en comparación al control que empezó con una población bacteriana base de 42x102 UFC/100 ml de coliformes fecales llegando hasta 5.24x108 UFC/100 ml (Figura 6).
El orden de remoción fue: S. auriculata = A. caroliniana > C. thalictroides > P. stratiotes > L. minor > S. intermedia > E. crassipes.
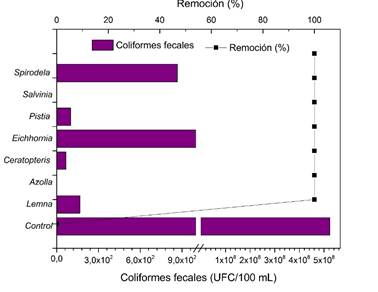

Figura 6 Efecto del bioensayo con diferentes especies de plantas sobre la concentración de coliformes totales en las aguas servidas. ▪ Indica el porcentaje de eficiencia de cada planta en la eliminación de coliformes totales.
En la Tabla 3 se muestra el inventario de plantas recomendadas para remoción de coliformes totales y E. coli en aguas servidas.
4. Discusión
Se seleccionaron plantas con potencial para eliminar coliformes totales y se verificó su capacidad para eliminar E. coli ATCC 25922. De las plantas estudiadas las más eficientes fueron: C. thalictroides, E. crassipes, P. stratiotes, S. auriculata y S. intermedia que eliminaron un 100% a la E. coli, valores superiores a los hallados por Neralla y Weaver (2000) quienes utilizaron la especie Typha latifolia y encontraron una eficiencia de remoción del 42.75%, sin embargo el tiempo de retención de estos autores fue menor (2 días) al empleado en el presente trabajo (7 días).
En relación con los coliformes totales las plantas acuáticas en siete días disminuyeron su concentración por debajo de los límites máximos permisibles (1000 NMP/100 ml) para agua de consumo humano, uso doméstico, riego y pecuario según el Acuerdo Ministerial 097A (2015).
La única especie que no eliminó en un 100% la población de coliformes fue E. crassipes, registrando 6433 UFC/100 ml. Estos resultados coinciden con los hallados por Rojas (2005), quien demostró que existen bacterias asociadas a E. crassipes tales como E. coli, Pantoea sp., Shigella sp., Klebsiella sp., Enterobacter cloacae, Pseudomona putida y Chromobacterium violaceum. Este autor también comparó la cantidad de bacterias asociadas a las raíces de plantas acuáticas de un humedal artificial para tratamiento de aguas servidas y demostró que E. crassipes presenta un mayor número de UFC/100 ml y una mayor diversidad de bacterias asociadas a sus raíces que P. stratiotes y A. caroliniana (Rojas, 2005).
Además, comparando los presentes resultados con los reportados por otros autores se observa que solo dos plantas S. auriculata y A. caroliniana alcanzaron una eficiencia del 100% en la eliminación de coliformes fecales, cercano al valor registrado para Phragmites australis que alcanzó un 99.7% y 99.6% en la remoción de E. coli y coliformes fecales, respectivamente (Mantovi et al., 2003).
Los factores que podrían haber influido en la remoción de bacterias como se demostró con el análisis de correlación fueron el pH, la temperatura, y la sedimentación. Según Solic y Krstuloviic (1992) el pH óptimo para la E. coli es de 6 - 7 y valores superiores provocan un declive en su población. Asimismo, Mayo (2004) apoya la teoría que a pH alcalinos mueren las coliformes fecales. En el experimento el pH en los controles sin las plantas se redujo de 8.20 a 7.40, por el contrario, en los tratamientos con las plantas el pH aumentó hasta 8.45 lo que podría haber promovido la muerte de las bacterias. Las especies que aumentaron el pH a 8.45 fueron A. caroliniana, y S. auriculata lo que explicaría su eficacia en la remoción de bacterias.
También hubo una reducción de la temperatura de 2 - 3 °C lo que también pudo haber influido en la muerte de las bacterias; ya que la temperatura óptima para el crecimiento de las coliformes es de 37 - 40 °C por lo que la reducción a 24 °C puede haber influido en su eliminación (Mayo, 2004).
También, la sedimentación pudo haber sido otro mecanismo de eliminación de bacterias, ya que las plantas podrían incidir en el incremento en la tasa de precipitación de sólidos suspendidos y disueltos en aguas servidas. En el ensayo de Zimmels et al. (2006) y en el presente trabajo se observó un aumento en la concentración de sólidos totales disueltos (TSD) al cuarto día del bioensayo, con una posterior disminución por precipitación. Además, se observó una correlación entre el TSD y la concentración de bacterias. En el estudio se apreció precipitación de material en suspensión y disuelto al cual podrían haberse unido las bacterias gram negativas por presentar una membrana externa compuesta por fosfolípidos y lipopolisacáridos que les confiere una carga electrostática negativa total a la pared celular (Buckley, Bender, Stahl, Martinko, y Madigan, 2015), por lo que podrían unirse a iones positivos de los sólidos disueltos y del material en suspensión.
El mecanismo de adsorción también pudo haber intervenido en la disminución de la concentración de coliformes. En este mecanismo las bacterias se unen a las raíces y actúan como un filtro natural. Se ha reportado que un gran número de coliformes se adhiere al cuerpo radicular de las macrófitas contribuyendo así a la eliminación de los coliformes y otros patógenos (Solano et al., 2004).
También se ha descrito que los exudados bactericidas generados por las raíces de las plantas aparte de ser tóxicos para las bacterias, pueden alterar el ambiente físico químico de la rizófora haciendo que esta sea inhabitable para futuras colonizaciones de bacterias patógenas (Akça et al., 2012). En este sentido se ha demostrado el efecto bactericida de extractos metanólicos y etanólicos de A. caroliniana contra las bacterias Enterococcus sp., Enterobacter aerogenes, E. coli y Pseudomonas aeruginosa (Nayak et al. 2015). Y en el caso de S. auriculata demostró actividad antibacterial contra E. coli, P. aeruginosa y S. aureus (Devi et al. 2015). Sin embargo, no se realizaron los ensayos para demostrar esta hipótesis, por lo que se propone para futuros trabajos analizar las bacteriocinas secretadas al agua por las plantas y su actividad antibiótica.
Además de la capacidad de eliminar coliformes totales y E. coli, los helechos acuáticos S. auriculata y A. caroliniana son capaces de acumular metales pesados y eliminar nitratos y fosfatos en aguas residuales según Caviedes et al. (2016) y Pernía et al. (2016), por lo que se propone el uso de estas especies para el tratamiento integral de las aguas servidas.
5. Conclusiones y recomendaciones
Las macrófitas C. thalictroides, P. stratiotes y L. minor fueron eficientes en la remoción de E. coli ATCC 25922 y coliformes totales en estudios in vitro y en aguas servidas, reduciendo la carga bacteriana por debajo de los límites máximos permisibles para agua potable y agua de uso agrícola. Las especies más eficientes fueron los helechos acuáticos A. caroliniana y S. auriculata los cuales removieron el 100% de las bacterias. Estas especies generaron variaciones sobre los parámetros fisicoquímicos que podrían estar involucrados en la eliminación de las bacterias.
Una vez analizados los resultados se acepta la hipótesis inicial de que existen plantas acuáticas capaces de eliminar coliformes totales y E. coli de las aguas servidas y se propone el uso de los helechos acuáticos A. caroliniana y S. auriculata para el saneamiento de aguas servidas previo a su vertido en ríos para minimizar la contaminación de los acuíferos.