Introducción
La leucemia linfoblástica aguda (LLA) es una neoplasia maligna caracterizada por la proliferación y acumulación de células progenitoras linfoides anormales en la médula ósea y/o en sitios extramedulares (1)(2).
El Registro Oncopediátrico Hospitalario Argentino (ROHA) realizado entre los años 2000 a 2008 calculó una incidencia de 45,7 casos por cada 1.000.000 de niños menores de 15 años por año (3). A pesar de afectar a infantes de todas las edades, la incidencia alcanza su punto máximo entre los 2 y 5 años, con un ligero predominio entre los varones (4).
El daño del SNC al momento del diagnóstico ocurre en 5 a 8% de los pacientes y se presenta con mayor frecuencia como alteración de nervios craneales o meningismo (5). La recaída del SNC ocurre en aproximadamente el 15% de los casos a pesar del tratamiento profiláctico, manifestándose como infiltración intraaxial, afectación meníngea o infiltración de la médula ósea, o las tres (6). Hay que destacar que la carcinomatosis meníngea (CM) ocurre en aproximadamente el 8% de las neoplasias malignas, siendo la causa más frecuente los tumores hematológicos, fundamentalmente la leucemia linfoblástica aguda y el linfoma no Hodgkin de grado intermedio o alto, y asociándose a mal pronóstico, con una supervivencia media entre 3 y 6 meses (7)(8).
El diagnóstico se establece por la presencia de 20% o más de linfoblastos en la médula ósea o la sangre periférica (9). La evaluación de la morfología, citometría de flujo, inmunofenotipaje y pruebas citogenéticas son valiosas tanto para confirmar el diagnóstico como para la estratificación del riesgo. La punción lumbar con análisis de líquido cefalorraquídeo (LCR) es el estándar de atención al momento del diagnóstico para evaluar el compromiso del SNC, estando indicado la realización de resonancia magnética cerebral y de neuroeje si el SNC está involucrado, sobre todo si existe CM asociada (1). Asimismo, el diagnóstico de compromiso del SNC por LLA surge de la visualización mediante microscopía de células leucémicas en LCR por citología convencional, que es considerado el método patrón oro. La evaluación de la morfología, citometría de flujo, inmunofenotipaje y pruebas citogenéticas son valiosas tanto para confirmar el diagnóstico como para la estratificación del riesgo. La punción lumbar con análisis de líquido cefalorraquídeo (LCR) es el estándar de atención al momento del diagnóstico para evaluar el compromiso del SNC, estando indicado la realización de resonancia magnética cerebral y de neuroeje si el SNC está involucrado, sobre todo si existe CM asociada (10).
El Grupo Argentino de Tratamiento de la Leucemia Aguda (GATLA) recomienda realizar examen del LCR al diagnóstico por citología convencional/recuento en cámara y cito-morfología por cytospin (CC), junto a datos clínicos y/o de neuroimagen (11).
El compromiso del SNC al diagnóstico confiere un peor pronóstico a la enfermedad y un mayor requerimiento de terapia dirigida a dicha localización. Además, las recidivas en SNC constituyen una de las razones principales de fracaso terapeútico durante el seguimiento a corto, mediano y largo plazo, estimadas entre 7-15%. Ciertas características de la neoplasia son consideradas factores de riesgo de compromiso del SNC al momento del diagnóstico, como el fenotipo B maduro, fenotipo T, BCR-ABL 1/Phi (+), hiperleucocitosis y LDH elevada, que permiten sospecharla, mientras que la recaída en SNC suele estar marcadamente asociada a fenotipo T, hiperleucocitosis, citogenético de alto riesgo como t(9;22) (q34.1;q11.2), BCR-ABL1, t(v;11q23.3), reordenamiento KMT2A, hipodiploidía, punción lumbar traumática y compromiso de SNC al diagnóstico (12).
Caso clínico
Varón de 20 años con antecedentes de sobrepeso grado I y de leucemia linfoblástica aguda de células B (LLA-B) BCR-ABL positivo a los 4 años tratado con inhibidores de la tirosín-quinasa (ITK). El paciente consulta en octubre de 2022 por un cuadro clínico de paraparesia flácida progresiva y trastorno sensitivo consistente en parestesias en miembros inferiores (MMII) de aproximadamente tres meses de evolución, con limitación funcional asociada y para la deambulación. El paciente niega síndrome febril, clínica respiratoria, abdominal ni otra focalidad neurológica asociada.
Exploración somática dentro de la normalidad.
Exploración neurológica:
-Balance motor según la Escala MRC (Medical Research Council) normal en miembros superiores. Balance motor por grupos musculares en miembros inferiores: en miembro inferior derecho cintura pelviana 2/5, bíceps semimembranoso y semitendinoso 1/5 y tibial anterior y flexión plantar 0/0. En miembro inferior izquierdo a nivel de cintura pelviana 1/5, bíceps semimembranoso y semitendinoso 1/5 y tibial anterior y flexión plantar 0/5.
-Reflejos miotáticos rotulianos abolidos y aquíleos hipoactivos. Reflejos cutáneo-plantares flexores.
-Trastorno sensitivo consistente en parestesias distales en cara externa de ambos miembros inferiores, asimétrico y de predominio izquierdo.
-Resto de exploración neurológica dentro de la normalidad.
Pruebas complementarias:
Bioquímica con perfil glucémico, ionograma, función renal y hepática, vitamina B12, ácido fólico, proteína C reactiva y procalcitonina dentro de la normalidad. LDH 413 U/l (10-250) y VSG de 56.00 mm/h (0.00-20.00). Coagulación normal.
Hematimetría con 7260 leucocitos/ul (3.00-12.00) con porcentaje de neutrófilos y linfocitos dentro de la normalidad.
Frotis de sangre periférica e inmunofenotipo con inmunoblastos de estirpe linfoide. Linfocitos activados con algunos de aspecto inmaduro. Del total de los leucocitos, 1.5% de blastos CD34+/CD19+/CD10+/CD20+(50%)/TDt+
Medulograma y estudio molecular: Presencia de hasta un 38% de blastos de fenotipo linfoide B aberrante. Médula ósea hipercelular con infiltración marcada por blastos de aspecto linfoide, compatible con infiltración por LLA preB y mutación BCR-ABLp190 (Figura 1). Mutación dominio ABL1 negativo. Cariotipo 46XY.
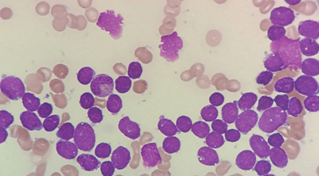
Figura 1 Estudio de extensión de médula ósea con tinción de Wright-Giemsa a 1000x donde se objetiva la presencia de células de gran tamaño con núcleo de cromatina laxa compatible con linfoblastos.
Resonancia magnética (RM) cerebral y de neuroeje: En el cráneo se observa captación leptomeníngea en surcos occipito-laterales izquierdos (Figura 2). En neuroeje se observa alteración de señal con captación de los somas toracolumbares y de los arcos costales como alteración de la hematopoyesis probablemente en el contexto de recaída tumoral. Además, se aprecia desde T11 hasta región sacra S1 proceso infiltrativo extramedular intrarraquídeo. Hallazgos neurorradiológicos compatibles con meningitis carcinomatosa e infiltración intraaxial extramedular intrarraquídeo de origen neoplásico.
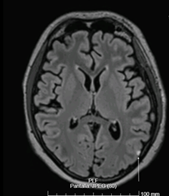
Figura 2 Resonancia magnética cerebral en secuencia FLAIR, corte axial. Captación hiperintensa a nivel leptomeníngeo en surcos occipito-laterales izquierdos.
PET-TC con 18F-FDG: Hallazgos que sugieren proceso lifnoproliferativo con afectación nodal supradiafragmática e infradiafragmática por presencia de foco hipermetabólico único peripancreático, asi como afectación medular D11-S1 en contexto de neurolinfomatosis (Figura 3).
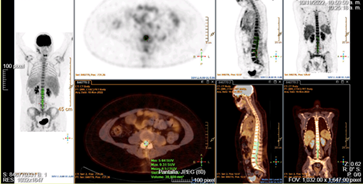
Figura 3 PET-TC con 18F-FDG con hallazgos con afectación medular D11-S1 en contexto de infiltración neoplásica axial extramedular intrarraquídea.
Electromiografía: datos compatibles con polineuropatía axonal motora, con afectación en miembros inferiores y presencia de denervación aguda.
Punción lumbar: ausencia de salida de LCR por infiltración medular metastásica en los 3 primeros intentos. Al cuarto intento LCR acelular sin presencia de blastos. BCR-ABL negativo. 69 copias de ABL.
Se confirma recaída de la enfermedad hematólogica tras realización de aspirado de médula ósea, se informa al paciente de los hallazgos y se procede a traslado desde Neurología a cargo de Hematología.
Evolución clínica:
Ante la situación clínica urgente que presenta el paciente, se decide iniciar tratamiento quimioterápico con el Bloque A con ciclofosfamida, doxorrubicina, vincristina y dexametasona, según esquema HCVAD (inicio 15/11/22) y posteriormente con Bloque B con metotrexato y citarabina a altas dosis. Como complicaciones presenta síndrome febril sin aislamiento microbiológicos e hipertransaminasemia transitoria en contexto hepatitis tóxica de origen farmacológico por quimioterápicos, con posterior resolución sin afectación a la función hepática. En la reevaluación tras el primer ciclo se objetiva buena respuesta, por lo que se inicia nuevamente tratamiento con Bloque A (inicio 13/12/22) con buena tolerancia. Por mal acceso intratecal, se coloca Reservorio Omaya el 14/12/22 para continuar el tratamiento.
Durante su estancia en planta de Hematología, el paciente se mantiene clínica y hemodinámicamente estable. Se realiza nuevamente un PET-TC tras quimioterapia 1 mes después, con importante mejoría de la captación en canal medular. Asimismo, se realiza aspirado de médula ósea de control 2 meses después del primer aspirado, que confirma remisión completa morfológica con 0.6% blastos y con BCR-ABL en sangre periférica y médula ósea negativos.
El paciente presenta una notable mejoría clínica neurológica, con capacidad autónoma para la deambulación y mejoría franca del balance motor, mejorando asimismo el trastorno sensitivo presente anteriormente.
Finalmente, el paciente recibe Dasatinib 140 mg de mantenimiento hasta nueva valoración por parte de Hematología.
Discusión
El caso clínico presentado destaca la complejidad y los desafíos que rodean el compromiso del sistema nervioso central (SNC) en la leucemia linfoblástica aguda (LLA). La recaída en el SNC es una complicación crítica, y su diagnóstico temprano es fundamental para un pronóstico favorable. El paciente experimentó una paraparesia flácida subaguda y una carcinomatosis meníngea que condujeron a una evaluación exhaustiva, incluyendo pruebas de imagen y análisis de líquido cefalorraquídeo, que confirmaron la afectación del SNC.
El tratamiento agresivo con quimioterapia, a pesar de las complicaciones temporales, resultó en una mejora significativa en los síntomas neurológicos y una remisión completa. Esto subraya la importancia de una atención multidisciplinaria y la necesidad de estrategias terapéuticas adaptadas a casos de LLA con compromiso del SNC.
Conclusiones
El interés de nuestro caso radica en la forma de presentación como primera recaída tardía de una leucemia linfoblástica aguda de estirpe linfoide B BCR-ABL. La paraparesia subaguda flácida por infiltración axial extramedular intrarraquídeo y la meningitis carcinomatosa por compromiso leptomeníngeo sincrónicos en contexto de una recaída leucémica tardía en un paciente adulto constituye un hallazgo muy poco frecuente y no se ha descrito actualmente en la literatura.














