Introducción
El accidente cerebrovascular (ACV) es una condición fisiopatológica caracterizada por la disminución transitoria o permanente, focal o global, del flujo sanguíneo en el cerebro (1). Representa un problema de salud pública en todo el mundo. Se estima que 1 de cada 20 muertes en Estados Unidos en el 2011 fue por un ACV y entre 2009-2012 el 2.6% de los estadounidenses ≥20 años padecieron esta patología, convirtiéndose en una de las enfermedades cardiovasculares con mayor morbilidad y mortalidad a nivel mundial (2). A través de los años se han buscado factores de riesgo modificables en los cuales impactar y realizar prevención de forma temprana, tales como tabaquismo, dislipidemia, hipertensión, la diabetes mellitus y la obesidad (3).
La obesidad ha sido identificada como una de las comorbilidades mayormente asociada a enfermedades cardiovasculares y por ende al accidente cerebrovascular. En estudios anteriores se ha calculado que más de 2.5 millones de personas mueren al año debido a la obesidad y el sobrepeso (4). Una de las principales causas de esta problemática es la fácil adquisición y accesibilidad en tiendas de cadena, restaurantes y colegios a alimentos procesados de alta densidad calórica y elevadas cantidades de azúcares y grasas, los cuales ayudan al aumento calórico diario (2). Sin embargo, muchos de estos productos incluyen entre sus componentes gran cantidad de fructosa, esto como resultado de la implementación del jarabe de maíz de alta fructosa (JMAF) en la industria alimentaria desde el siglo pasado (4), que por sus grandes capacidades edulcorantes se logró utilizar menor cantidad para lograr el mismo objetivo que se tenía con el azúcar convencional y conseguir niveles de glucosa plasmática más bajos de los que registraban con los consumos de sacarosa (5).
Previos estudios han demostrado que el alto consumo de fructosa magnifica la lesión por isquemia cerebral en un modelo experimental, esto visto en regiones tales como la corteza motora y el hipocampo que son consideradas áreas de penumbra isquémica (4) así como un déficit en el desempeño motor y de memoria y aprendizaje de los animales sometidos a la dieta (6). Adicionalmente, se ha estimado desde el punto de vista microestructural a partir del tercer día de la isquemia, se ha reportado una disminución de la inmunorreactividad en dendritas y el soma neuronal de la proteína asociada a microtúbulos 2 (MAP2) en regiones directamente afectadas por el cese de riego sanguíneo (7).
Sin embargo, la isquemia también produce cambios en el tejido cerebral en áreas que no están relacionadas con la zona de isquemia. Dichos cambios han sido denominados “cambios exofocales” provocados por señales químicas o eléctricas que se originaron del foco isquémico (7). Numerables estructuras son consideradas zonas exofocales, entre ellas, la amígdala, una estructura pequeña situada en el lóbulo temporal que juega un papel importante en la memoria y en el procesamiento emocional en el marco del reconocimiento expresivo, auditivo y conductual de las emociones (8); tal procesamiento es dirigido por un conjunto de circuitos anatómicos y conexiones complejas como las proyecciones y señales sensoriales (9). Previos estudios han demostrado alteración morfológica en la amígdala luego de una isquemia cerebral, a través de la caracterización histológica por Nissl (10). Estas zonas exofocales son poco valoradas y generalmente las consecuencias funcionales se observan tiempos tardíos post-infarto. Por lo tanto, el objetivo de la presente investigación es determinar el efecto del alto consumo de fructosa sobre la inmunoreactividad de MAP2 en la amígdala en un modelo animal de isquemia cerebral.
Materiales y métodos
Animales
Ratas albinas Wistar hembras de cuatro meses de edad con un peso de 240 a 360 g fueron utilizadas en el presente estudio. Las ratas fueron criadas y alojadas en las instalaciones de animales en SIU (Sede de Investigación Universitaria), Universidad de Antioquia, Medellín, Colombia. Las ratas fueron mantenidas en un ciclo de luz/oscuridad de 12:12 h y recibieron comida y agua ad libitum. Cuatro o cinco animales fueron alojados por caja. Todos los experimentos con animales fueron aprobados por el Comité de Ética de Experimentación Animal de la Universidad de Antioquia, sede Medellín, Colombia, y se realizaron de conformidad con las normas colombianas (ley 84/1989 y resolución 8430/1993).
Dieta
Los animales fueron divididos en dos grupos según el peso inicial para asegurar que ambos grupos de animales iniciaran con el mismo peso promedio. Los dos grupos fueron: control y HFD. El grupo de control recibió agua normal y el grupo HFD recibió de forma “ad libitum” 20 % de fructosa en agua (D(−)-fructosa (USP, BP, Ph. Eur.) grado farmacéutico durante 11 semanas. Ambos grupos fueron alimentados con alimento estándar (Laboratory Autoclavable Rodent Diet 5010, LabDiet, St Louis, MO, USA) durante las 11 semanas. El consumo de agua (ml) y alimento (g) fueron registrados cada dos dias.
Modelo de isquemia cerebral
Después de 11 semanas de dieta, los animales en los grupos de control y HFD se dividieron aleatoriamente en subgrupos simulados e isquémicos: sham control (n = 5), sham HFD (n = 5), isquemia control (n = 5) e isquemia HFD (n = 5). Las ratas se anestesiaron con ketamina (90 mg/kg) y xilazina (5 mg/kg) y recibieron una mezcla de isoflurano al 2-4 % y oxígeno al 96 % a través de una máquina de anestesia por inhalación. Se implementó una variación en el modelo isquémico cerebral global, a saber, una oclusión de 2 vasos (2-VO). La arteria carótida común (CCA) derecha se ocluyó permanentemente con una sutura de nylon de calibre 6,0 y la CCA izquierda se obstruyó durante 20 min con un clip vascular. Después de 20 min, se retiró el clip vascular para permitir la reperfusión. Las ratas simuladas se sometieron al mismo procedimiento sin la oclusión de CCA.
Análisis histológico
Los animales fueron sacrificados, los cerebros se extrajeron cuidadosamente y se fijaron posteriormente. con paraformaldehído al 4% a 4°C durante 48 h, seguido de conservación con un gradiente de sacarosa (7, 25 y 30%) a 4ºC; Luego, los cerebros se colocaron en una crioconservación. solución a -20°C. Se realizaron cortes coronales de 50 μm obtenidos con un vibratomo (VT1000STM, Leica Microsystems, Nussloch, Alemania). El bregma seleccionado para el análisis histológico de la amígdala fue de -3,12. Para la inmunotinción, las secciones se permeabilizaron con Tritón X100 al 0,3 % y se bloquearon con BSA al 1 %. en PBS, usando protocolos previamente descritos para inmunohistoquímica para el anticuerpo primarios evaluado anti-MAP2 (monoclonal de ratón, Sigma-Aldrich Cat# M1406, RRID:AB_477171, 1:1000). Los cortes de la amígdala fueron analizados usando el microscopio Zeiss Axio Scope A1 y fotografiados en 40X y 100X utilizando una cámara Zeiss AxioCam ERc 5s. Las imágenes fueron modificadas a un sistema binario ImageJ (versión 1.8.0) y se obtuvo la densidad integrada (unidades relativas) de cada imagen utilizando el mismo software.
Resultados
La isquemia y el alto consumo de fructosa generan pérdida de la inmunoreactividad de MAP2
Nosotros encontramos que, tanto el grupo isquemia control como el grupo isquemia con alto consumo de fructosa tuvieron reducción de la inmunoreactividad de MAP2 en el hemisferio derecho (Figura 1A), lo cual fue corroborado cuando se realizó la cuantificación, donde se observa que dicha reducción es estadísticamente significativa (Figura 1B). Sin embargo, el hemisferio izquierdo no presentó disminución estadísticamente significativa de dicha inmunoreactividad en los grupos isquémicos comparados con el control (Figura 1B). Adicionalmente, tampoco se encontró una diferencia entre los valores de inmunoreactividad de los animales sham control con respecto a los valores de los animales sham con alto consumo de fructosa (Figura 1)
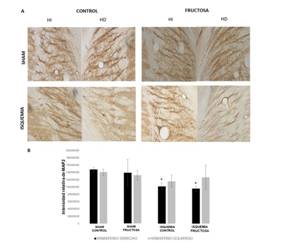
Figura 1 Pérdida de inmunorreactividad de MAP2 producto de la isquemia. A. Fotografías de inmunohistoquímica de MAP2 del hemisferio derecho e izquierdo de la amígdala (10x). B. Cuantificación de la inmunoreactividad de MAP2. n = 4, *p < 0.05.
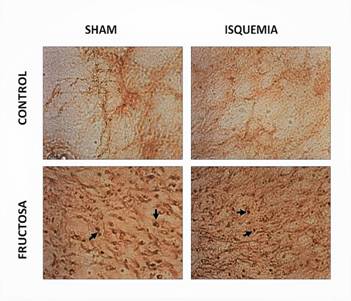
El alto consumo de fructosa genera cambios morfológicos en las dendritas
Teniendo en cuenta que los resultados más relevantes estuvieron enmarcados en el hemisferio derecho, secciones de cerebro de dicho hemisferio fueron observadas y analizadas en mayor detalle en 100x. Se observan unos puntos más oscuros de inmunoreactividad de MAP2 a lo largo de las dendritas tanto en el grupo sham que consumió fructosa, como en el grupo isquémico que consumió fructosa, si estos son comparados con el grupo sham control (Figura 2, cabezas de flechas). Adicionalmente, en el grupo isquemia control se observa poca inmunoreactividad (Figura 2), lo cual soporta el resultado anteriormente mostrado en la figura 1.
Discusión
La fisiopatología del daño neuronal y la pérdida de las ramificaciones dendríticas a nivel estructural y conformacional debido a la obstrucción del flujo sanguíneo se encuentra bien establecida. Este evento comienza con un fracaso energético ocasionado por la interrupción de gradientes iónicos, lo que conlleva a acumulación de calcio intracelular y formación de radicales libres de oxígeno. Estos fenómenos moleculares en conjunto con los procesos inflamatorios propician un ambiente de acidosis y apoptosis celular en el tejido neuronal lo que incrementa el daño de la lesión y el cambio progresivo en la morfología neuronal (11). Dicha morfología a nivel del citoesqueleto es dada principalmente por microfilamentos, filamentos intermedios y microtúbulos, estos últimos se ubican especialmente en las dendritas y son organizados por las proteínas asociadas a microtúbulos (MAP2) (11)(12).
Cambios y alteraciones significativas en la configuración morfológica de las dendritas frente a un ACV han sido ampliamente reportados (13)(14). Mages y colaboradores en el 2021 encontraron reducción de MAP2 asociada a la isquemia de forma temprana y uniforme en la zona focal isquémica, en comparación con los controles (15). Otro estudio realizado en el año 2020 con modelos animales de isquemia cerebral encontró reducción en la longitud de las dendritas y daño neuronal en la corteza cerebral (16). Estos hallazgos argumentados en la literatura son congruentes con los resultados obtenidos en este estudio, donde se observó pérdida en las dendritas a las 48 horas post-isquemia en la región de la amígdala, reflejados mediante inmunohistoquímica en la reducción significativa de MAP2.
Adicionalmente, nosotros encontramos que ratas que sufrieron una isquemia cerebral y que consumieron altas cantidades de fructosa de igual manera tuvieron pérdida significativa de MAP2 en la amígdala del hemisferio derecho. Pérez y colaboradores en 2020 encontraron el mismo hallazgo, pero en regiones de hipocampo y corteza cerebral (4), lo que indica que no solo en la amígdala ocurren cambios ante estos eventos sino también en otras estructuras cerebrales (10). En este mismo estudio se encontró que los animales obesos producto del consumo de fructosa tenían una mayor pérdida de inmunorreactividad NeuN en diferentes áreas del cerebro a las 48 h post-isquemia (4). De hecho, la pérdida de inmunorreactividad de MAP2 y NeuN en dicha investigación estuvo asociada a la pérdida de inmunomarcaje de otros marcadores de plasticidad como el factor neurotrófico derivado del cerebro (BDNF) y aumento en la respuesta astrocitaria e inflamatoria (4).
El consumo de fructosa o también llamado jarabe de maíz es una gran problemática a nivel mundial, se ha relacionado con un aumento de la obesidad y trastornos metabólicos siendo relacionado con los factores de riesgo de enfermedad cardiovascular, en especial el accidente cerebrovascular (17). Un estudio demostró que después de haber sometido a las ratas a un alto consumo de fructosa se presentó reducción de aproximadamente 40% de la neurogénesis cerebral; en nuestro estudio pese a que no se encontró reducción significativa de la inmunoreactividad de MAP2 en el grupo sham fructosa, sí se observan acúmulos de inmunoreactividad en dicho grupo, lo cual nos puede sugerir alteración de las dendritas producto del solo consumo de fructosa (18).
Estos acúmulos o puntos más intensos a lo largo de las dendritas es la primera vez que se ha reportado bajo estas condiciones, sin embargo, otros autores relacionan este fenómeno con la gravedad de la lesión isquémica focal aguda (4).
Se ha demostrado que la amígdala cumple funciones en la memoria, en el procesamiento emocional y en el reconocimiento expresivo y conductual de las emociones, como lo son el miedo y el placer (8)(19). Se han estudiado en modelos animales las repercusiones funcionales del daño a nivel de la amígdala donde se ha encontrado por medio de pruebas de funcionamiento cognitivo en los roedores que en tiempos tardíos de isquemia la depresión y la ansiedad son las principales consecuencias neuropsiquiátricas después de un ACV (20). Estos hallazgos animales son respaldados por estudios en humanos donde encontraron que los pacientes con accidente cerebrovascular presentaron déficit cognitivo asociado a una reducción significativa del tamaño de la amígdala (21) De los muchos trastornos posteriores al ictus, la depresión, la ansiedad, la incontinencia emocional, la propensión a la ira y la fatiga son síntomas frecuentes e importantes (22). Por lo tanto, los análisis realizados en la región de la amígdala son importantes ya que, ante un evento cerebrovascular las estrategias terapéuticas en gran medida están enfocadas en realizar rehabilitación en las fases agudas puesto que es un periodo crucial donde se ha encontrado mejor respuesta al tratamiento, omitiendo muchas veces las repercusiones tardías como son las alteraciones en las emociones y la depresión post isquemia (23).
Este estudio muestra que alteraciones histológicas posteriores a una isquemia y producto de alto consumo de fructosa afectan de manera importante la estructura dendrítica de la amígdala lo cual podría estar relacionado con los cambios emocionales en los pacientes que sufren ACV como se discutió anteriormente y, con el impacto emocional que genera la recurrencia del consumo de azúcares en nuestro día a día.
Conclusiones
La isquemia a través de un modelo global de 2-VO y, el alto consumo de fructosa generan pérdida de la inmunoreactividad de MAP2 en amígdala en un modelo experimental. Adicionalmente, el alto consumo de fructosa a su vez genera cambios morfológicos en las dendritas de dicha región. Por lo tanto, no solo un evento isquémico sino el consumo elevado de fructosa en la dieta desencadena daño dendrítico de la amígdala lo cual podría estar representado de forma tardía en posibles alteraciones emocionales y de memoria, evaluaciones funcionales que podrían ser tenidas en cuenta en futuros estudios.