Introducción
La Parálisis Cerebral (PC) es la causa más frecuente de discapacidad infantil. Engloba un grupo de trastornos permanentes, pero no invariables, del movimiento y la postura que provocan limitación de la actividad, causados por interferencias, anormalidades o lesiones cerebrales no progresivas que ocurren en el cerebro inmaduro o en desarrollo.
Aunque la definición de PC ha ido cambiando a lo largo del tiempo(1) el diagnóstico sigue siendo clínico y se debe acompañar de más información que ayude a conocer la afectación del niño (tipo de trastorno motor, función motora, distribución anatómica, trastornos asociados, etc.) (2).
Los niños con PC van a asociar, en la mayoría de los casos, además de los problemas neurológicos, otros trastornos no neurológicos que serán más frecuentes a mayor grado de afectación de la PC.
Objetivo
El objetivo de esta revisión es recopilar, de forma ordenada, los principales problemas que pueden desarrollar estos pacientes para que los profesionales que atienden a niños con PC conozcan cuáles son, cómo identificarlos y cómo abordarlos en caso necesario.
Epidemiología
La PC es una de las enfermedades más prevalentes y la causa de discapacidad más frecuente en pediatría, sobre todo en países desarrollados. La prevalencia general es de 1.5-3 por cada 1.000 recién nacidos vivos(4) .
Etiología
La PC puede derivar de cualquier evento que altere el desarrollo del cerebro fetal o neonatal. Las principales causas y factores de riesgo relacionados aparecen en la Tabla 1(4)(5).
Tabla 1 Causas y factores de riesgo de la PC.
| PRENATAL | PERINATAL | POSTNATAL |
|---|---|---|
| Factores maternos: Ingesta de tóxicos Infección intrauterina Traumatismo Disfunción tiroidea, HTA Alteraciones de la coagulación Enfermedades autoinmunes Fecundación in vitro o técnicas de reproducción asistida | Desprendimiento de placenta Corioamnionitis Prematuridad, bajo peso Infección SNC o sistémica Hipoglucemia grave/mantenida Hiperbilirrubinemia Hemorragia intracraneal Hipoxia neonatal Crisis neonatales | Infecciones Traumatismo craneal Parada cardiorespiratoria Intoxicación Deshidratación grave Estatus convulsivo Asfixia |
| Factores placentarios: Trombosis/oclusión, hipoperfusión infección/inflamación | ||
| Factores fetales: Malformaciones SNC Eventos vasculares SNC Síndrome genético Enfermedad metabólica CIR Gestación múltiple |
*HTA: Hipertensión arterial, SNC: Sistema nervioso central, CIR: Crecimiento intrauterino retardado.
Clasificación
El concepto de PC engloba un grupo de pacientes muy heterogéneo. Según el tipo de trastorno motor las clasificamos en espástica (la más frecuente), discinética, atáxica, hipotónica o mixtas. Según el área corporal afectada distinguimos: tetraplejia/tetraparesia, paraplejia/paraparesia, cuadriplejia y monoplejia/monoparesia. Existen escalas para valorar de forma objetiva el grado de dependencia y la funcionalidad de los niños con PC(6) (Tabla 2):
-Escala GMFCS (Gross Motor Function Classification System) para función motora gruesa.
-Escala MACS (Manual Ability Classification System) para función motora fina.
-Escala CFCS (Communication Function Classification System) para comunicabilidad y el lenguaje.
Tabla 2 Escalas de valoración de grado de dependencia y funcionalidad en la PC.
| GMFCS | MACS | CFCS | |
| I | Marcha sin restricciones pero limitada para las actividades motoras más demandantes | Utiliza objetos con facilidad y con éxito | Envía y recibe información eficaz y eficientemente con personas conocidas y desconocidas |
| II | Marcha con restricciones | Utiliza la mayoría de los objetos, pero con una calidad del movimiento reducida o con menor velocidad en la realización | Envía y recibe información de forma eficaz pero de forma más lenta con conocidos y desconocidos |
| III | Marcha con asistencia técnica que utiliza con las manos | Utiliza los objetos con dificultad necesitando ayuda en la preparación o realización de actividades | Envía y recibe información de manera eficaz sólo con personas conocidas |
| IV | Limitaciones para la automovilidad, puede utilizar una asistencia técnica controlada por el paciente | Manipulación limitada a una selección de objetos en un entorno adaptado | Envía y/o recibe información de manera inconsistente con personas conocidas |
| V | El paciente necesita ser transportado por otra persona en una silla de ruedas | No maneja objetos o tiene limitaciones muy importantes para realizar actividades simples | Casi nunca envía y/o recibe información |
Tasas de supervivencia
La esperanza de vida de los niños con PC depende de la gravedad de esta, la supervivencia disminuye cuanto mayores son la afectación motora y problemas asociados (discapacidad intelectual, disfagia, desnutrición, etc.). En la PC leve (GMFCS I-II) la supervivencia es del 99% a los 20 años, sin embargo, en la PC grave (GMFCS V) es del 40%. Los problemas respiratorios son la causa de muerte más frecuente en todas las series(7)(8).
TRASTORNOS NEUROLÓGICOS
Epilepsia:
Entre el 35-62% de los niños con PC desarrollan epilepsia. Ésta es más frecuente en los niños con hallazgos patológicos en la neuroimagen y mayor afectación motora. La epilepsia de niños con PC tiene unas características diferenciales: mayor incidencia de epilepsia con inicio dentro del primer año de edad, antecedentes de convulsiones neonatales, estatus epiléptico, necesidad de politerapia y tratamiento con fármacos antiepilépticos de segunda línea(9). Además, estos pacientes tienen con más frecuencia crisis focales, crisis reflejas, síndromes epilépticos graves y diferentes tipos de convulsiones a lo largo de la evolución de su epilepsia(10). La realización de un EEG estaría indicado ante la sospecha de crisis de posible origen epiléptico, y el inicio de tratamiento se valorará de forma individualizada en cada caso en función del riesgo de recurrencia de las mismas.
Trastornos del movimiento:
Se sabe poco sobre su prevalencia, aunque se han descrito hasta en un 40%, y hasta en un 10% coexisten más de un tipo de movimiento anormal(11). Son más frecuentes en la PC discinética, y a menudo aparecen en combinación con espasticidad. Producen mucha afectación funcional ya que interfieren o incluso imposibilitan la realización de las actividades de la vida diaria, además de causar dolor.
El más frecuente es la distonía, muy incapacitante, que consiste en la contracción desordenada de agonistas y antagonistas en un movimiento intencionado. El tratamiento de la distonía incluye la terapia física como piedra angular, fármacos orales como trihexifenidilo y levodopa (Tabla 3), la infiltración local de toxina botulínica (en la distonía focal) y, en algunos casos, tratamiento quirúrgico con infusión intratecal de baclofeno para la espasticidad asociada o estimulación cerebral profunda (aún en investigación en el caso de PC).
Tabla 3 Fármacos usados para el tratamiento de trastornos del movimiento y espasticidad en niños con PC.
| Fármaco | Dosis inicial | Dosis máxima | Efectos adversos |
| Trastornos del movimiento: Trihexifenidilo | 0.1 mg/kg/día en 3 dosis | 0.5 mg/kg/día o 10 mg/día | Trastornos del sueño, mareo, cefalea, xerostomía, estreñimiento. |
| Levodopa | 1 mg/kg/día en 3-4 dosis | 10 mg/kg/día. | Anorexia, xerostomía, insomnio, discinesias, alteraciones hematológicas. |
| Tetrabenazina | 12,5 mg/día | 150 mg/día | Sedación, sialorrea, bradicinesia, disartria, pérdida de fuerza. Riesgo de síndrome neuroléptico maligno |
| Levetiracetam | 5 - 10 mg/kg/día | Somnolencia, irritabilidad, labilidad emocional. | |
| Espasticidad: Baclofeno | 0,5 mg/kg/día, en 3-4 tomas. | 40 mg/día en < 2 años 60 mg/día en 2 - 6 años 120 mg/día en > 6 años | Somnolencia, hipotonía, xerostomía, estreñimiento |
| Tizanidina | 0,1-0,2 mg/kg/día, en 2 - 3 tomas. | 36 mg/día | Somnolencia, hipotensión, bradicardia, xerostomía, debilidad muscular |
| Clonidina | 0,025 mg-0,05 mg/día | 0,2-0,3 mg/día. | Xerostomía, estreñimiento Bradicardia, hipotensión. Somnolencia. |
La corea y la atetosis son menos frecuentes, pero pueden coexistir y en determinados casos ser el trastorno principal. Clásicamente para el tratamiento se ha empleado la tetrabenazina, el levetiracetam puede ser una opción terapéutica eficaz en algunos casos(12) (Tabla 3).
Discapacidad intelectual:
Presente entre el 40-70% de los niños con PC en grado variable. Mayor en espástica y en cuadriplejia. Peor si presenta epilepsia, un EEG o un estudio de neuroimagen anormal(9).
Trastornos del lenguaje:
La disartria (alteración en la articulación del lenguaje) es el más frecuente (40%), sin embargo, el 25% de los niños con PC serán incapaces de producir lenguaje inteligible. El objetivo del tratamiento es maximizar en los niños la capacidad de comunicarse a través del habla, los gestos o las herramientas complementarias (como los dispositivos de comunicación) que necesiten, para permitir que se conviertan en comunicadores independientes. Debe abordarse de forma individualizada y precoz (idealmente antes de los 2 años) (13)(14).
Problemas neuropsiquiátricos:
Pueden estar presentes en más del 50% de los niños con PC, sin embargo, muchos de ellos no son valorados por los servicios de salud mental infantil. Incluyen trastornos emocionales, problemas de conducta y en la interacción social, hiperactividad/falta de atención, que agravan los problemas escolares y adaptativos, lo que provoca gran angustia y dificulta la integración del niño en su entorno(15).
PROBLEMAS ORTOPÉDICOS
Espasticidad:
Presente en el 85% de los niños diagnosticados de PC(16).
Produce un desequilibrio de fuerzas que da lugar a una disminución del movimiento articular, lo que origina contracturas y deformidades osteoarticulares(17).
El abordaje de la espasticidad resulta complejo y debe ser individualizado. La finalidad es intentar mejorar la funcionalidad, favorecer la higiene, disminuir el dolor y prevenir complicaciones. Debe tenerse en cuenta que la espasticidad no tratada afecta tanto al niño como al cuidador y aumenta el coste de los cuidados médicos(18).
Su enfoque incluye fisioterapia, terapia ocupacional, ayudas técnicas como férulas y órtesis, farmacoterapia oral con baclofeno, tizanidina, clonidina, benzodiacepinas (Tabla 3) y fármacos de administración parenteral con efecto local como la toxina botulínica y bloqueos nerviosos(19). Entre los tratamientos quirúrgicos se encuentran las técnicas de neuromodulación (infusión intratecal de baclofeno) que permiten mayor eficacia con menos efectos secundarios generales, y las técnicas neurolesivas (neurotomía o rizotomías selectivas).
Deformidades osteoarticulares:
Entre las deformidades osteoarticulares(19) más frecuentes nos encontramos con los pies equinos (60-80%), el desplazamiento o luxación de cadera (35%) y la escoliosis (20-25%), la prevalencia aumenta considerablemente en el GMFCS IV-V(20)(21). La cirugía ortopédica tiene como objetivo reequilibrar las fuerzas en torno a la articulación, y corregir las deformidades. Se puede actuar sobre las partes blandas (micro/tenotomías, transferencias tendinosas) o sobre las partes óseas (osteotomías, artrodesis). Es recomendable realizar la mayoría de los procedimientos como un solo evento de cirugía de múltiples niveles para minimizar los riesgos. Además, este enfoque permite planificar mejor la rehabilitación postoperatoria(18).
TRASTORNOS DIGESTIVOS
Los problemas gastrointestinales crónicos van a estar presentes en un 80-90% de los pacientes(22).
Malnutrición:
La malnutrición en el niño afecto de PC tiene un origen multifactorial y está descrita en un 60-90% de los pacientes. Está originada por la disfunción orofaríngea, escasa ingesta, déficit de micronutrientes y, raramente, aumento de necesidades (PC tipo disquinética, enfermedades intercurrentes o crisis epilépticas). Otras comorbilidades que dificultan la alimentación son debidas a la dismotilidad: reflujo gastroesofágico, náuseas, retraso del vaciamiento gástrico y estreñimiento(23). Debemos satisfacer los requerimientos nutricionales del paciente identificando los trastornos digestivos precozmente y minimizando los riesgos asociados, ya que los problemas digestivos empeoran el pronóstico neurológico y la calidad de vida de estos pacientes(24).
Se debe realizar una valoración nutricional donde se incluya la anamnesis, encuesta dietética y antropometría. La valoración antropométrica del niño con PC constituye un verdadero desafío y será la principal herramienta para valorar si la nutrición está siendo adecuada. Aunque existen gráficas específicas para niños con parálisis cerebral según género y según nivel de GMFCS(25) tiene especial importancia ver la progresión individual monitorizando su propia curva de crecimiento(26).
En el abordaje nutricional del niño con PC siempre usaremos la vía más fisiológica: vía oral con alimentación tradicional. Si precisa usaremos enriquecimiento natural preferentemente con grasas que permiten aumentar calorías en poco volumen o suplementos nutricionales orales.
Disfagia:
La disfagia va a estar presente en torno a un 40%-90% de los niños con PC(27)(28). La succión débil, incoordinación en la succión-deglución, cierre ineficiente de labios y masticación ineficaz conlleva -en muchos casos- aumento del tiempo de ingesta y en algunos un inadecuado aporte calórico. La disfunción orofaríngea conlleva riesgo de aspiración broncopulmonar de contenido alimentario con empeoramiento del estado respiratorio del paciente. En caso de sospecha de disfagia debemos evaluar seguridad y eficacia de la deglución mediante observaciones de la ingesta y videofluoroscopia si procede. El abordaje de la disfagia incluye la modificación de texturas con espesantes o cambios de posturas durante las comidas (papel importante de logopeda). Si lo anterior fracasa y la vía oral no es segura o no es eficiente optaremos por alimentación enteral mediante sonda nasogástrica o gastrostomía(22).
Reflujo gastroesofágico:
Está presente en un 50-75% de los pacientes con PC. La etiología es multifactorial: alteraciones de la postura, dismotilidad neurológica con aumento de relajaciones transitorias de esfínter esofágico inferior y aumento de la presión abdominal secundario a espasticidad y escoliosis. Debemos sospecharlo ante la presencia de síntomas como rechazo de la ingesta, vómitos, hipersalivación, complicaciones respiratorias u otros síntomas inespecíficos como irritabilidad, anemia o alteraciones dentales. Puede ser útil la realización de ph-impedanciometría. En casos leves pueden beneficiarse de espesar las comidas y mantener incorporado tras la ingesta. Si no, los inhibidores de la bomba de protones constituyen la primera línea de tratamiento y en casos refractarios evaluar la indicación de técnicas quirúrgicas. (22).
Estreñimiento:
La alteración de la postura y el tono, ingesta deficiente de líquidos, la inmovilidad o la ingesta de fármacos origina que alrededor de la mitad de los pacientes presenten estreñimiento. Origina complicaciones gastrointestinales relacionadas con la dismotilidad e infecciones urinarias de repetición. Para el tratamiento se precisa en un primer momento la desimpactación (evitando en este momento alto contenido en fibra) y posteriormente tratamiento de mantenimiento con polietilenglicol o lactulosa junto con medidas dietéticas(22).
PROBLEMAS RESPIRATORIOS
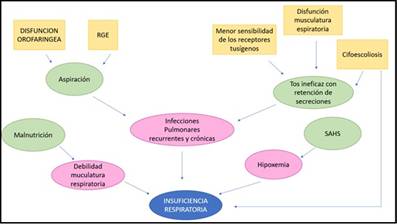
La prevalencia y la intensidad de la afectación respiratoria se relacionan con la gravedad de la afectación motora, presentando neumonías recurrentes hasta el 70% de los niños con PC tetrapléjica. Múltiples factores se ven implicados en la afectación respiratoria de los pacientes con PC (Figura 1) (29)(30)(31): alteración de los mecanismos protectores de la vía aérea superior (VAS), aspiración recurrente, disfunción respiratoria de origen central, cifoescoliosis y alteraciones morfológicas de la caja torácica que condicionan un tórax restrictivo, alteración del tono muscular, alteraciones respiratorias durante el sueño (las alteraciones respiratorias del sueño originan hipercapnia y posteriormente hipoxemia, con riesgo de desarrollo de hipertensión pulmonar).
Al valorar al niño con PC debemos realizar una aproximación diagnóstica con la anamnesis, el estudio de la función pulmonar y el estudio de hipoventilación(32).
En cuanto a las medidas de prevención la vacunación supone el pilar fundamentar, por lo que debemos indicar la vacunación antigripal estacional desde los 6 meses de edad, la vacunación antineumocócica con esquemas mixtos que incluyen la VNC13 y la VNP23 y la administración de palivizumab estacional en menores de 2 años con hipotonía marcada o compromiso respiratorio grave.
El tratamiento de los principales problemas respiratorios irá dirigido a la optimización del tratamiento broncodilatador, mejorar el aclaramiento secreciones, antibioterapia precoz en caso de sospecha de infección respiratoria bacteriana y el uso de la VNI en Síndrome de apneas-hipopneas del sueño, hipercapnia o desaturación.
SALUD ÓSEA:
Los niños con PC presentan riesgo de baja densidad mineral ósea (DMO) y osteoporosis. La inmovilidad, baja ingesta de micronutrientes (calcio y vitamina D), la desnutrición y la terapia anticonvulsivante contribuyen a su aparición. (33). Las fracturas patológicas pueden estar presentes hasta en un 20% de los pacientes, afectan con más frecuencia a fémur distal y ocasionan un empeoramiento de la calidad de vida(34). La densitometría por absorciometría dual de rayos X (DEXA) es la técnica más empleada para medir la densidad mineral ósea. Para hablar de osteoporosis se precisa la presencia de baja DMO junto con historia de fracturas clínicamente significativas o fracturas por compresión vertebral en ausencia de enfermedad local o traumatismo de alta energía donde estarían indicados los bifosfonatos(35)(36).
PROBLEMAS VISUALES
Entre un 40 y 75% de los niños que padecen PC tienen algún grado de discapacidad visual. Dicha discapacidad es un factor contribuyente clave para el deterioro de la función locomotora y cognitiva en la PC con problemas de percepción que dificultarán el aprendizaje, particularmente cuando no se identifica y se actúa sobre ella(37)(38).
Algunos de los signos que nos alertan de posibilidad de afectación visual(38)(39) son el nistagmo, comportamientos como frotarse repetidamente los ojos o balanceos repetitivos de la cabeza o el tronco, la ausencia de parpadeo o retirada ante estímulos luminosos y “amenaza” (objeto que se acerca rápidamente), la realización de movimientos oculares suaves, pero sin finalidad, y la falta de atención y curiosidad visual.
PROBLEMAS AUDITIVOS
La prevalencia de alteraciones auditivas en niños con PC varía entre el 4 y el 13%.
La afectación auditiva se relaciona con el desarrollo del lenguaje, y éste, con la capacidad de comunicación y trastornos del comportamiento. También afecta a la capacidad de aprendizaje en caso de no ser detectadas y tratadas de manera precoz(40). Las infecciones respiratorias de vías altas de repetición pueden originar pérdida de audición intermitente que de no ser tratadas adecuadamente pueden originar sordera permanente. En la anamnesis debemos incluir factores de riesgo de sordera (antecedentes familiares, causa de parálisis cerebral, empleo de fármacos ototóxicos) y recoger el comportamiento auditivo y el desarrollo del lenguaje. Constituyen signos de alerta la escasa respuesta a estímulos auditivos, respuesta comportamentales anómalas o alteración del desarrollo del lenguaje.
TRASTORNOS UROLÓGICOS
Hasta el 60% de los pacientes presentan disfunción miccional (vaciado incompleto de la vejiga con residuo postmiccional), enuresis, urgencia miccional, incontinencia o vejiga neurógena. Debemos tratar de alcanzar la continencia en todos los pacientes, con independencia de la afectación(41). Entre las medidas higiénico dietéticas destaca la adecuada ingesta de líquidos (1500 ml/m2), el tratamiento del estreñimiento y la alarma de enuresis. El tratamiento farmacológico incluye el uso de anticolinérgicos y la desmopresina. En caso de vejiga neurógena, el tratamiento de elección es el sondaje vesical intermitente.
DESARROLLO PUBERAL Y PROBLEMAS SEXUALES:
El desarrollo puberal en niños no deambulantes con GMFCS III-IV o V se produce de manera diferenciada a la población normal: los primeros signos de desarrollo puberal aparecen antes tanto en niñas como en niños, pero el tiempo para completar el desarrollo de caracteres sexuales secundarios es más prolongado(42)(42).
En niños con PC y nivel de inteligencia conservado tanto el interés sexual como la práctica sexual se inician de forma más tardía, pero se iguala a los 20 años de edad. Algunas causas limitantes de las relaciones sexuales se relacionan con la gravedad de la afectación motora, el grado de dependencia para la movilidad independiente y con la capacidad de establecer relaciones sociales(44).
No podemos olvidar que las personas con discapacidad tienen hasta 3 veces más riesgo de ser víctimas de abusos sexuales, siendo múltiples los factores favorecedores de esta situación por lo que la educación sexual debe estar incluida en la educación de los niños con PC e incluirse en la historia de salud el abordaje a la sexualidad, detectando problemas que puedan precisar intervención para su mejoría.
SALUD BUCODENTAL:
Las malformaciones orofaciales, bruxismo, predominio de dietas blandas, la presencia de reflujo gastroesofágico o la higiene deficiente originan que en torno a un 50% de los niños con PC presenten caries, maloclusiones y enfermedad periodontal. Por otro lado, suele ser un colectivo con menor demanda de asistencia bucodental(45).
El papel de la prevención primaria mediante la educación familiar en higiene dental es primordial por lo que debemos insistir en el cepillado dental tras cada comida por parte del cuidador con pasta dental con adecuada cantidad de flúor. Además, debe realizarse exploración bucodental rutinaria y en caso de detectar patología derivación a especialista en odontología para sellado, obturaciones, exodoncias y tartrectomías.
SIALORREA:
La prevalencia de sialorrea en niños con PC varía entre el 10 y el 58%(46).
La sialorrea en los niños con PC no es a causa de una producción excesiva de saliva sino debido a la disfunción motora de la fase oral de la deglución con un cierre inadecuado de los labios, a los movimientos de la lengua desorganizados y exacerbados por la falta de percepción sensorial oral y perioral, a la postura de cabeza hacia abajo y a la disfagia.
Es necesario cuantificar tanto la frecuencia y la gravedad de la sialorrea (escala de Thomas-Stonell y Greenberg(47)), como su impacto en la calidad de vida de los niños y sus cuidadores (Escala Drooling Impact(48)).
Los objetivos principales en el tratamiento de la sialorrea son: la reducción del impacto socio-afectivo y de salud causados por la sialorrea anterior; la reducción del impacto en la salud causados por sialorrea posterior; mejorar la calidad de vida para pacientes y cuidadores; y la reducción de la carga que experimentan los cuidadores. En cuanto a las principales medidas diferenciamos: el entrenamiento de la conciencia sensorial y las habilidades motoras orales, la terapia farmacológica con fármacos de primera línea como el bromuro de glicopirronio o la escopolamina y la infiltración de toxina botulínica, dejando la cirugía sólo para casos graves donde otras opciones no han tenido resultados(49).
TRASTORNOS DEL SUEÑO
Los trastornos del sueño están presentes en el 25% de los niños con PC en comparación con el 5% de la población general. Los principales trastornos del sueño en niños con PC son las dificultades para iniciar y mantener el sueño nocturno, el despertar matutino difícil, las pesadillas y la ansiedad del sueño(50).
Cuando los niños experimentan falta de sueño evidencian alteraciones del estado de ánimo, del comportamiento y cognitivas. Los trastornos del sueño son también una de las principales razones para el estrés en los padres que tienen hijos con enfermedades crónicas o discapacitados, influyendo todo lo anterior en la calidad de vida percibida tanto del niño como su familia.
Para identificar si existen estos trastornos con una anamnesis dirigida (diario de sueño) será suficiente, aunque en algunos casos seleccionados podrá ser necesaria la realización de un electroencefalograma (por su asociación con crisis epilépticas) o una polisomnografía(51).
En cuanto al abordaje, las familias deben conocer los principios generales y asegurar una correcta higiene del sueño. También, se pueden considerar varios agentes farmacológicos, los más avalados en este grupo poblacional son melatonina y melatonina/triptófano; benzodiacepinas (lorazepam): eficaz en la inducción del sueño aunque tienden a inducir tolerancia farmacológica y dependencia; o fármacos derivados de las benzodiacepinas como zolpidem.
DOLOR:
El dolor es un síntoma frecuente, algunos estudios sugieren prevalencia de hasta el 32% de los niños(52) y el 74%(53) en jóvenes con PC.
El dolor que experimentan los niños con PC tiene un efecto negativo en su vida diaria que puede conllevar a la expresión de angustia, ansiedad, depresión, irritabilidad, insomnio, fatiga y comportamientos negativos de afrontamiento no sólo en ellos sino también en los demás miembros de la familia.
La identificación, evaluación y tratamiento del dolor en niños con PCI sigue siendo en la actualidad un verdadero desafío debido, sobre todo, a ser poco explorado en la anamnesis, a los problemas de comunicación de los pacientes y a la limitación en las herramientas de medición. Esto nos obliga a buscar sistemáticamente la existencia y los desencandenantes del dolor.
Los mecanismos más frecuentes(54) que generan dolor en esta población incluyen tanto el dolor nociceptivo: somático (espasticidad, subluxación de la cadera, fractura…) y visceral (estreñimiento, reflujo gastroesofágico, úlcera gástrica…), como el dolor neuropático; sin poder olvidarnos del dolor secundario a tratamientos: fisioterapia, infiltración de toxina botulínica… Además, es frecuente que en los niños con PC coexistan al mismo tiempo varias fuentes de dolor.
El dolor será más frecuente y más grave a mayor grado de GMFCS(55). Entre las herramientas para la evaluación del dolor recomendamos el uso de r-FLACC(56) por su facilidad de uso y sus cualidades pragmáticas.
En cuanto al tratamiento debemos comenzar con una evaluación integral, con el objetivo inicial de identificar y tratar la causa siempre que sea posible. Para la elección del fármaco más apropiado contamos con las directrices de la Organización Mundial de la Salud sobre el tratamiento farmacológico del dolor persistente en niños con enfermedades médicas(57), sin olvidar el enfoque multimodal.
ASISTENCIA PSICOLÓGICA, SOCIAL Y EDUCATIVA:
Se debe establecer un plan de atención al paciente apoyando a los cuidadores y dotándolos de las competencias necesarias para participar activamente en el desarrollo vital del niño afecto de PC.
Conclusiones
En las últimas dos décadas el enfoque del paciente con PC ha cambiado, pasando de estar únicamente dirigido al niño hacia un enfoque familiar. Sin embargo, las familias se siguen mostrando en muchos casos insatisfechas con la atención recibida(58). Los niños con PC tienen necesidades de atención médica complejas y a menudo requieren atención por un equipo multidisciplinar, sin embargo, en base a nuestra experiencia resulta evidente que un pediatra debe coordinar todo el seguimiento que estos niños necesitan y por tanto, estar familiarizado con los principales problemas de estos niños y sus tratamientos.