INTRODUCCIÓN
La diabetes mellitus tipo 2 es una enfermedad con niveles de afectación poblacional en continuo y alarmante aumento. En Ecuador, la prevalencia de diabetes en la población entre 20 y 79 años es de 4.7% 1. El sobrepeso y la obesidad se encuentran entre los principales factores de riesgo, observándose en los últimos años un aumento de la prevalencia de obesidad entre niños y adolescentes 2. El indicador de sobrepeso y obesidad en la población infantil (5- 11 años) es del 35,38% y en la población adolescente (12-19 años) es del 29,57% 3. La diabetes mellitus tipo 2 está vinculada a trastornos metabólicos de la glucosa, de los triglicéridos (TAG) y del colesterol total, por lo que su oportuna detección a través del análisis clínico es importante para la prevención en salud 4. En 2021, el gasto relacionado con la diabetes en Ecuador fue de USD 2280,5 por persona 1.
Los resultados de las pruebas clínicas deben ser fiables y comparables para asegurar la eficaz gestión del paciente 4, tanto en términos de salud pública como de costos económicos. Del 60% al 70% de las decisiones médicas se basan en los resultados de las pruebas de diagnóstico in vitro 5, que dependen del método de análisis y muchas veces no pueden ser comparables entre distintos laboratorios 4.
La falta de fiabilidad provoca la repetición innecesaria de ensayos y el consiguiente gasto de salud pública evitable 5. La inadecuada utilización de las pruebas de laboratorio en cualquier etapa del proceso (pre analítica, analítica y post análitica), pueden conducir a resultados erróneos que ponen en peligro la salud y seguridad del paciente 6. El análisis de concordancia permite establecer la validez de una nueva técnica de medición o calificación diagnóstica o demostrar la equivalencia de múltiples técnicas de medición o calificación 7,8.
Varios estudios de comparación de resultados clínicos entre laboratorios se han llevado a cabo en otros países. Se ha comparado la precisión diagnóstica de pruebas sanguíneas, incluyendo colesterolemia, para la evaluación de la fibrosis hepática frente a la biopsia hepática, en pacientes no tratados con hepatitis crónica tipo C 9. Gialamas y col. 10 en su estudio de los resultados de varios parámetros clínicos, entre ellos el colesterol total y los niveles de TAG, obtuvieron una concordancia entre el 85 y 89%. Un estudio de reproducibilidad de los valores de concentración de iones metálicos en la sangre de pacientes con implantes de metal en la cadera, llevado a cabo por Rahmé y col. 11, han indicado que existen diferencias significativas entre laboratorios, debido a las diferentes tecnologías utilizadas para las mediciones. Kramer y col. 12 evaluaron la reproducibilidad de nuevos parámetros de respuesta a la insulina y la glucosa en la prueba de tolerancia oral a la glucosa (OGTT) y su relevancia fisiopatológica tanto en individuos sanos como en diabéticos. Un análisis de la concordancia del tratamiento antibiótico de pacientes con sepsis grave produjo un alto grado de concordancia, lo cual determinó menos reingresos a la Unidad de Cuidados Intensivos 13. Un estudio de la concordancia entre los resultados obtenidos con un analizador de gases en sangre y con un analizador automático en la medición de hemoglobina y electrolitos en pacientes críticamente enfermos, demostró que los resultados fueron moderadamente concordantes, por lo que ambos métodos no podían intercambiarse 14. Los errores comunes en el proceso de análisis de pruebas de laboratorio fueron estudiados por Nerenz y col. 6, quienes también examinaron varias prácticas establecidas para maximizar los beneficios de los resultados de estas pruebas.
Sin embargo, en Ecuador no existe suficiente evidencia científica sobre la similitud de los resultados obtenidos en diferentes laboratorios clínicos pese a que se ha utilizado la misma técnica de análisis. Entonces, el objetivo de este trabajo fue realizar un estudio comparativo de los resultados obtenidos en diferentes laboratorios de los principales marcadores de la diabetes: glucosa, TAG y colesterol total.
La calidad de una medida depende tanto de su validez como de su fiabilidad 15, que indica hasta qué punto se obtienen los mismos valores medir en más de una ocasión, bajo condiciones similares 16,17. La concordancia entre variables clínicas es afectada por la variabilidad de los observadores, por la variabilidad del instrumento de medida o por el propio proceso a medir 16,18. Para remplazar una antigua técnica de medida será necesario que la nueva técnica sea suficientemente concordante 19,20. Suele utilizarse la correlación lineal, pero puede ser engañoso 19,21, pues este concepto no es igual al de concordancia 22. Altman & Bland 20, proponen un gráfico sencillo para evaluar la concordancia entre dos métodos de medida, representando la diferencia entre cada pareja de valores frente a su media 19,20,22. El coeficiente de correlación intraclase estima el promedio de las correlaciones entre todos los pares de observaciones y se emplea para cuantificar la fiabilidad de las mediciones de variables cuantitativas continuas 16,23. La tasa de concordancia se puede determinar mediante el análisis actuarial que calcula la proporción de pares concordantes sobre la suma de pares concordantes y discordantes 24. Cerda J. y Villarroel L. 25 evaluaron la concordancia entre observadores en investigación pediátrica explicando la forma correcta de interpretar el valor del coeficiente kappa de Cohen.
Con estos antecedentes, el objetivo en este estudio fue determinar estadísticamente la concordancia de los valores de colesterol, glucosa y triglicéridos obtenidos en cuatro laboratorios clínicos distintos de la ciudad de Riobamba.
II. MATERIALES Y MÉTODOS
Procedimiento experimental
Se extrajeron cuatro muestras de sangre utilizando tubos al vacío sin aditivo de 5 mL, a 61 voluntarios en ayunas (46 mujeres y 15 hombres) con edades comprendidas entre 19 y 22 años. Las muestras de cada voluntario se colocaron en cuatro diferentes coolers con temperatura controlada y fueron inmediatamente transportados a cuatro laboratorios seleccionados para los análisis de colesterol, glucosa y triglicéridos, evitando agitarlos bruscamente para impedir la hemolización de la sangre.
Materiales y métodos
En cada uno de los cuatro laboratorios clínicos se realizaron los análisis de colesterol, glucosa y triglicéridos mediante el método espectrofotométrico utilizando un equipo semiautomático calibrado según los procedimientos de cada laboratorio. Se ha realizado un análisis descriptivo por género. Se ejecutó el análisis de varianza de un factor (LABORATORIO), previa verificación de los supuestos de homocedasticidad y de normalidad, para comparar las medias de los resultados, seguida por la prueba de Tukey para la determinación de los subconjuntos homogéneos. Con los valores de los parámetros clínicos se realizó la correlación lineal, se adaptó el análisis de Bland-Altman para comparación interlaboratorios y se determinó el coeficiente de correlación intraclase. Para determinar la concordancia se calcularon las frecuencias y porcentajes de los resultados clínicos dentro y fuera del rango referencial 10. Todos los análisis estadísticos se llevaron a cabo utilizando IBM® SPSS® Statistics 22 y los gráficos con SigmaPlot 12.
III. RESULTADOS Y DISCUSIÓN
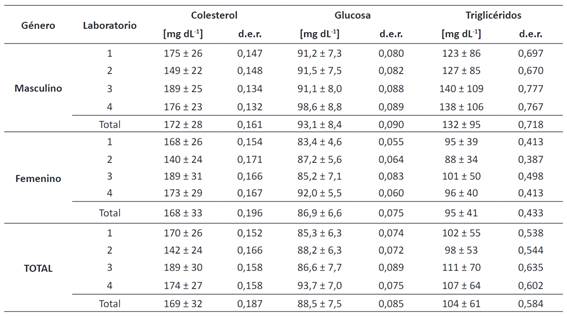
Los triglicéridos presentan mayor variabilidad con valores de desviación estándar relativa (d.e.r.) entre 0,387 y 0,777; mientras que la menor variabilidad se observa en los valores de glucosa 0,055 ≤ d.e.r. ≤ 0,089. En general, el laboratorio 1 muestra los resultados más homogéneos y el laboratorio 3 los menos homogéneos.
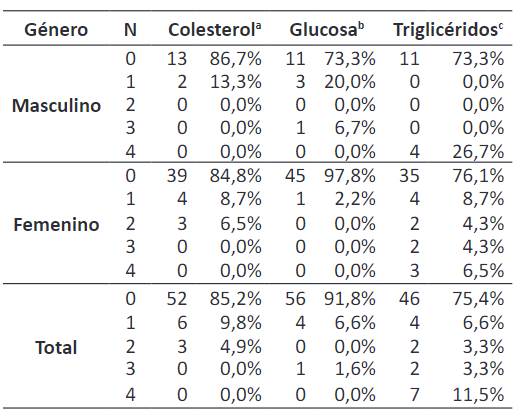
De igual forma, los resultados de glucosa (0,090) y triglicéridos (0,718) son más variables en hombres, en tanto que los resultados de colesterol (0,196) son más variables en mujeres (Tabla 1).
La Tabla 2 muestra que los laboratorios 1, 4 obtuvieron valores similares de colesterol, pero significativamente diferentes de los resultados de los laboratorios 2, 3. Los valores de glucosa son similares para los laboratorios 1, 2 y 3 pero muy diferentes de los valores encontrados en el laboratorio 4. Los valores medios de triglicéridos son similares para todos los laboratorios.
Tabla 2 Comparación por laboratorio. a
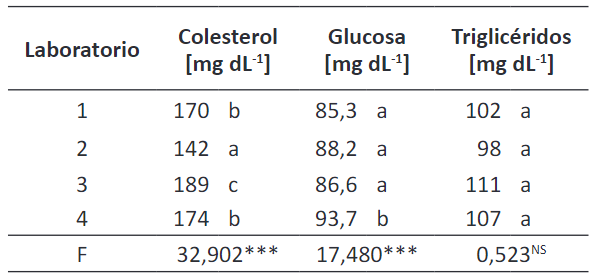
a Los valores seguidos por la misma letra no presentan diferencia significativa.
***: diferencia significativa a P < 0.001; NS: no significativa.
La Tabla 3 muestra los valores del coeficiente de correlación lineal (r), del coeficiente de correlación intraclase (CCI) y del coeficiente kappa de Cohen (k) para cada pareja de laboratorios y cada parámetro analizado. El análisis de correlación lineal muestra que todos los pares de laboratorios están significativamente correlacionados con p < 0,01. De acuerdo con la tabla de valoración de la concordancia según los valores del CCI 16, existe buena concordancia en los triglicéridos con un CCI promedio de 0,891, y moderada concordancia en glucosa (CCI promedio = 0,616) y colesterol (CCI promedio = 0,599). Considerando la fuerza de la concordancia 25, en general los triglicéridos presentan una concordancia considerable, la glucosa tiene concordancia aceptable, y el colesterol exhibe una leve concordancia. Se puede observar que una buena correlación lineal no conduce necesariamente a una buena concordancia.
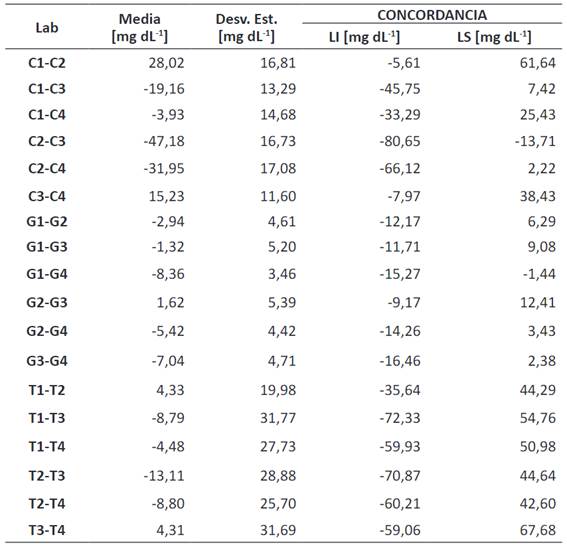
En la Tabla 4 se pueden observar los límites de concordancia obtenidos por el método de Bland-Altman. Los resultados de glucosa son los que presentan límites de concordancia más bajos, pero en general los intervalos son muy amplios, denotando falta de concordancia de las medidas interlaboratorios.
Tabla 3 Correlaciones y concordancias entre laboratorios.
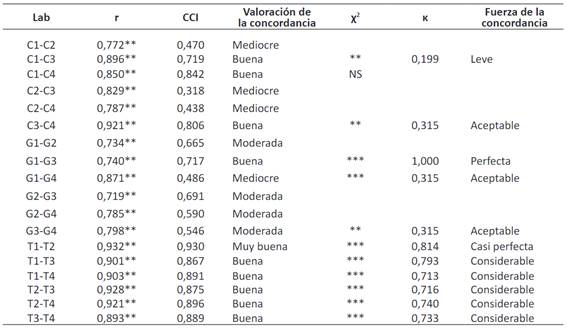
r: coeficiente de correlación lineal, CIC: coeficiente de correlación intraclase,
χ2: chi cuadrado, κ: coeficiente kappa de Cohen.
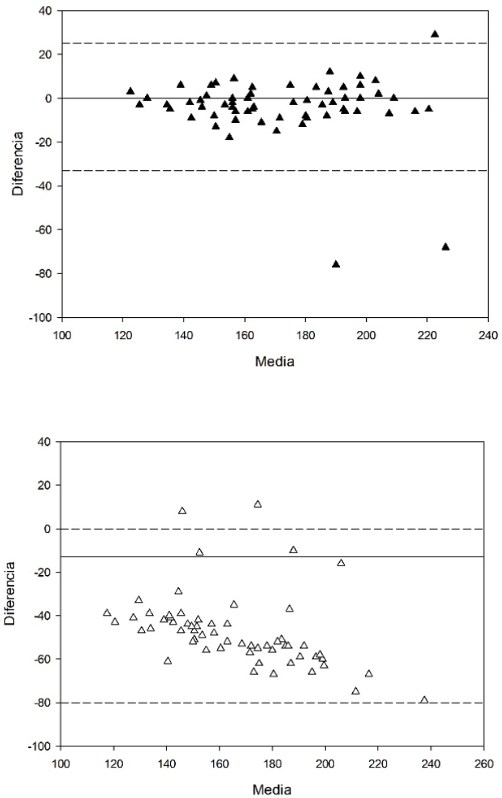
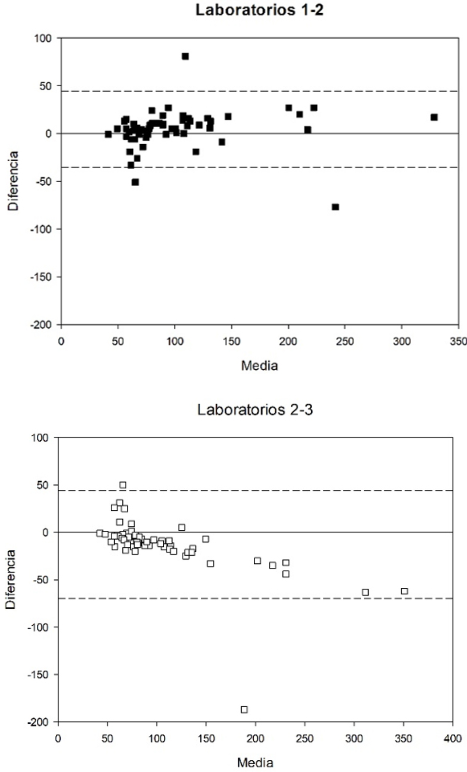
En la Figura 1 se muestran los gráficos de Bland-Alman para colesterol. A la izquierda está el caso con mayor concordancia, con diferencia media de -3,9 mg dL-¹ y límites de concordancia del 95% (-33,3 y 25,4 mg dL-¹). A la derecha se encuentra el caso con menor concordancia con diferencia media de -47,2 mg dL-¹ y límites de concordancia del 95% (-80,7 y -13,7 mg dL-¹).
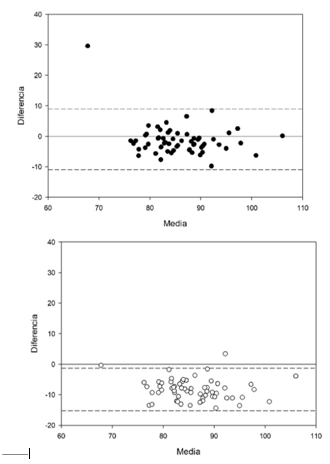
En la Figura 2 se muestran los gráficos de Bland-Alman para glucosa. A la izquierda está el caso con mayor concordancia, con diferencia media de -1,3 mg dL-¹ y límites de concordancia del 95% (-11,7 y 9,1 mg dL-¹). A la derecha se encuentra el caso con menor concordancia con diferencia media de -8,4 mg dL-¹ y límites de concordancia del 95% (-15,3 y -1,4 mg dL-¹).
En la Figura 3 se muestran los gráficos de Bland-Alman para triglicéridos. A la izquierda está el caso con mayor concordancia, con diferencia media de 4,3 mg dL-¹ y límites de concordancia del 95% (-35,6 y 44,3 mg dL-¹). A la derecha se encuentra el caso con menor concordancia con diferencia media de -13,1 mg dL-¹ y límites de concordancia del 95% (-70,9 y 44,6 mg dL-¹).
En general, los casos con mayor concordancia muestran una diferencia media mucho menor y un rango menos amplio. Los valores se distribuyen uniformemente alrededor de la media esperada de cero. En todos los casos con menor concordancia se nota una tendencia hacia debajo de la media esperada.
En la Tabla 5se observa el número de laboratorios que presentan valores fuera del rango normal para un mismo individuo. Los resultados coincidentes conducen al mismo diagnóstico, mientras que los no coincidentes pueden llevar a diagnósticos equivocados. Las coincidencias de los resultados de colesterol, glucosa y triglicéridos son del 85,2%, 91,8% y 86,9%, respectivamente. Valores similares fueron obtenidos por Gialamas y col. 10 que reportaron concordancias entre 85 y 89% para colesterol y triglicéridos.
IV. CONCLUSIONES
Todos los pares de laboratorio están correlacionados linealmente, pero esto no significa que exista concordancia.
El 14,8% de los resultados respecto a colesterol (13,3% en hombres y 15,2% en mujeres), 8,2% respecto a glucosa (26,7% en hombres y 2,2% en mujeres), y 13,1% respecto a triglicéridos (0,0% en hombres y 17,4% en mujeres) podrían conducir a un diagnóstico médico equivocado debido a la falta de coincidencia entre los resultados de los diferentes laboratorios en los cuales se realizan los análisis clínicos.
Los órdenes de concordancia considerando tanto el CCI como el k de Cohen son similares: triglicéridos > glucosa > colesterol.
Para mejorar la concordancia de los resultados de diferentes laboratorios, sería necesario tener procesos de acreditación de laboratorios.
En el futuro se podrían ampliar los estudios comparativos a otros parámetros clínicos, considerando laboratorios a nivel nacional y en diferentes grupos etáreos.