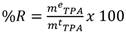INTRODUCCIÓN
En el 2018, la producción de plásticos en todo el mundo alcanzó 343 millones de toneladas. Siguiendo esta tendencia, se estima que en 20 años la producción se incremente y se fabriquen 1 100 millones de toneladas de este material 1. En el mismo año, alrededor de 292 millones de toneladas cortas de desechos sólidos municipales fueron generados tan solo en Estados Unidos y de este universo, el 12,2% (35,7 millones de toneladas estadounidenses) representaba a los plásticos. De este último porcentaje, el 79% estaba distribuido de la siguiente manera: Polietileno de baja densidad, LDPE (30,3%). Polipropileno, PP (28,8%). Polietileno de alta densidad, HDPE (22,2%) y PET (18,7%) 2. Claramente se evidencia un consumo excesivo.
El desecho inadecuado de residuos representa un alto riesgo para la supervivencia de la vida silvestre, se han registrado muertes de animales provocadas por la ingesta de plásticos 3. Diversos Gobiernos han incorporado políticas a favor de combatir la problemática ambiental. Algunos Estados han planteado incorporar ciertos porcentajes de materiales reciclados como materia prima, para la creación de nuevos productos 4 y otros Estados incluso han vetado la adquisición de plásticos de un solo uso 5.
Entre los diferentes tipos de plásticos disponibles en el mercado, la investigación se focalizó en el plástico tipo PET. Dicho polímero es un termoplástico utilizado por las fábricas para elaboración de envases, paquetes de alimentos y botellas 6. De acuerdo con el informe emitido por Smithers Pira, el mercado mundial de envases PET elaboró aproximadamente 16,4 millones de toneladas. En los próximos 5 años se estima que la demanda de estos envases aumente en 4,6% cada año 7.
El plástico PET se podría considerar como un agente nocivo para el planeta debido al mal uso post consumo que se le da al ingresar grandes cantidades de este residuo en vertederos municipales, a su alta resistencia a los agentes biológicos y atmosféricos, además por no ser un plástico degradable a condiciones normales 8. La radiación UVB de la luz solar, las propiedades hidrolíticas del agua del mar y las propiedades oxidativas de la atmósfera hacen que los desechos plásticos en mares y océanos se desintegren en micropartículas; incluso en el 2018 con el estudio realizado por la Agencia Austriaca de Medio Ambiente se encontraron residuos de PP y PET en heces humanas 9.
Este tipo de plástico se puede recuperar mediante incineración y reciclaje. La incineración no es una vía ecológica, debido a la emisión de gases tóxicos y la presencia de cenizas residuales cuya composición incluye cadmio y plomo. El método más respetuoso con el medio ambiente que da la preservación de los materiales y la energía es el reciclaje 10.
El reciclaje es una alternativa para minimizar la cantidad de residuos plásticos en vertederos; con las tecnologías que se disponen hoy en día, tan solo en Europa más del 50% de los plásticos, entre ellos PET, llegarían a ser potencialmente reciclables por una vía ecoeficiente 11. Sin embargo, a los países subdesarrollados se dificulta el llegar a un correcto tratamiento debido a la falta de conocimiento y apoyo tanto técnico como económico 12.
Existen dos métodos principales de reciclaje: método mecánico y químico. El reciclaje mecánico es el más común, aproximadamente el 84% del PET es reciclado, recolectado, clasificado, limpiado y por último se procede a la molienda 13. Estos últimos pasos pueden ir en orden diferente, dependiendo de la composición y el origen del plástico 14.
En el reciclaje químico se rompen las cadenas que forman el polímero, este proceso se desarrolla por medio de solvólisis o termólisis. La glicólisis, metanólisis, hidrólisis, aminólisis y demás, son algunas alternativas que se presentan en la solvólisis 15. En la despolimerización del PET por medio de hidrólisis (ácida, neutra o alcalina) se obtienen como productos: etilenglicol (EG) y TPA. El ácido oxálico también es factible sintetizarlo por medio este mecanismo 16. Entre las variables que afectan al rendimiento se encuentran: el tiempo de reacción, efecto de la concentración de la base, temperatura, tamaño de partícula, entre otros 17.
Por medio de la hidrólisis alcalina, las sales tereftálicas son hidrolizadas empleando ácido clorhídrico (HCl) o ácido sulfúrico (H2SO4) hasta formar TPA. Comúnmente, se emplea hidróxido de potasio (KOH) o hidróxido de sodio (NaOH) con una concentración de 4%-20% en masa 18. En la hidrólisis ácida se obtiene rendimientos altos, pero debido al alto consumo de ácido, esta vía se convierte en un proceso muy costoso y altamente corrosivo. Además de que tiene un efecto negativo en la pureza del EG. Por otro lado, con la hidrólisis neutra, a pesar de no ser una vía nociva, todas las impurezas presentes en el plástico se manifiestan en el TPA, por lo cual afecta su pureza 19.
La presente investigación tuvo como objetivo identificar cómo el tamaño de partícula interfiere en el rendimiento de la hidrólisis alcalina de PET. El plástico de color se dimensionó en dos tamaños T5mm y T10mm. Para la hidrólisis se empleó NaOH, agua (H2O) y EG, el proceso necesitó 120°C por 30 minutos. Se trabajó con un sistema hermético para evitar pérdidas de masa. El TPA se caracterizó por medio de la espectroscopia FT-IR y prueba de solubilidad.
MATERIALES Y MÉTODOS
Equipos
Para la caracterización de la materia prima (PET) así como del producto despolimerizado, se usó el espectrofotómetro infrarrojo modelo “JASCO FT/ IR-4100”, resolución 0,9 cm-¹ rango de número de onda 7800-350 cm-¹. Para la hidrólisis se emplearon: balanza analítica “OHAUS EXPLORER, EX 224” con una sensibilidad de 0,1mg; Agitador magnético con plancha de calentamiento “THERMO FISHER SCIENTIFIC” rango de velocidad 60-1110 l/min y temperatura máxima de 450°C; Bomba al vacío “DOA-P704” modelo GM-05, presión máxima de 60psig; Bureta digital “Hirschmann solarus, 9392020”, rango de temperatura 4°C-50°C y precisión 0,2%; pH-metro “OAKLON 2700” rango (-2.000 a 20.000)pH y exactitud ±0,002+1 LSD; Estufa “POL-EKO, SRN 115” temperatura máxima 250°C y convección de aire natural.
Caracterización del plástico
Diariamente durante tres semanas se recolectaron muestras provenientes de zonas exclusivas para el reciclaje de plásticos dentro de las instalaciones de la ESPOCH, con preferencia por aquellos materiales que presentan un color distintivo. Las muestras se rasparon hasta obtener un polvo fino, el cual se analizó en el espectrofotómetro.
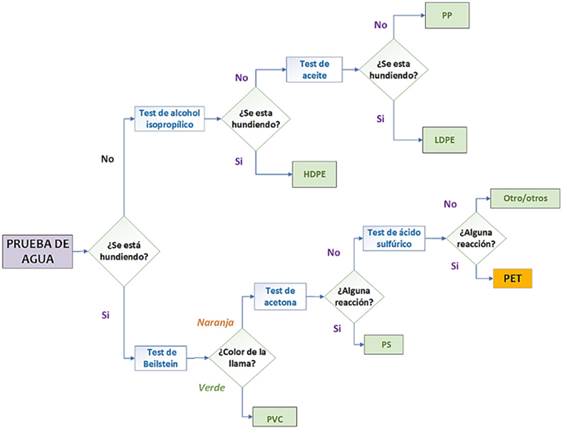
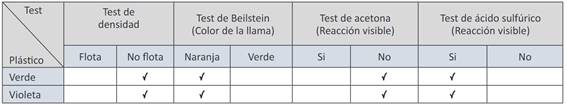
Siguiendo el esquema de la Figura 1, el test clásico de identificación de PET consiste en cuatro fases: test de densidad, test de Beilstein, test de acetona y test de ácido sulfúrico. Para el test de densidad, se requiere de 2mL de agua destilada dentro de un tubo de ensayo conjuntamente con las muestras del polímero. Se registra: ¿Flota o no Flota? En el test de Beilstein es necesario usar un cable de cobre enrollado en la muestra y acercar el sistema a una fuente de calor. Se observa el color de la llama.
Finalmente, en el test de acetona y de ácido sulfúrico, se emplean 6mL de cada reactivo concentrado dentro de dos tubos de ensayo diferentes, conjuntamente con el plástico. Además, para el último test es necesario someter el sistema a baño María por media hora, se retira y se deja enfriar la muestra. Se registra: Alguna reacción visible ¿Si o No? Una vez identificado el material, se colocó una criba en el triturador para tener una abertura apropiada y poder dimensionar las láminas en: (T5mm) y (T10mm).
Hidrólisis alcalina
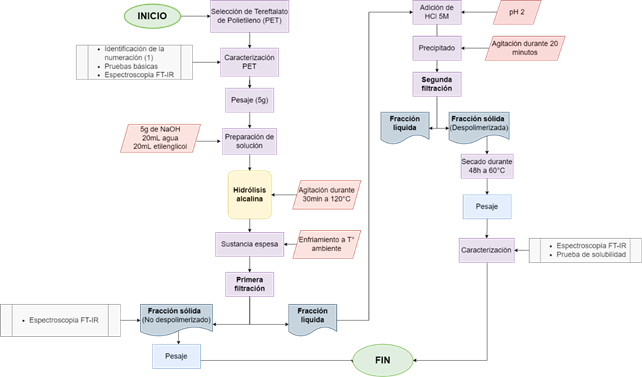
5g de plástico, previamente lavado y triturado, se mezcló con 5g de NaOH, 20mL de H2O y 20mL de EG 22. La despolimerización se desarrolló dentro de un vaso de precipitación de 250mL completamente hermético, bajo las siguientes condiciones:
Al final de la reacción, se obtuvo una sustancia espesa color melón (plástico violeta) y color verde (plástico verde). La metodología restante se desarrolló acorde lo estipula el trabajo de Kandasamy et al. 22. Con la diferencia que, para la neutralización se usó HCl 5M y para el secado, se programó la estufa a 60°C durante 48 horas.
Caracterización
Las muestras sólidas despolimerizadas y las no despolimerizadas se analizaron en el espectrofotómetro. Además, para la prueba de solubilidad es necesario colocar 5mL de cada reactivo en un tubo de ensayo conjuntamente con 1 g de la muestra obtenida de la hidrólisis. Los cinco reactivos son: agua destilada, etanol, hexano, ácido acético y cloroformo.
Rendimiento (%)
Se realizaron un total de 16 experimentaciones. El porcentaje de rendimiento se calculó acorde a la Fórmula 1:
%R = Rendimiento expresada como porcentaje
Me = Masa experimental final en gramos de TPA.
Mt = Masa teórica final en gramos de TPA.
Para 5 gramos de PET usados en la hidrólisis alcalina se espera teóricamente 4,3225g de TPA 23.
III. RESULTADOS Y DISCUSIÓN
Pruebas básicas de identificación de PET
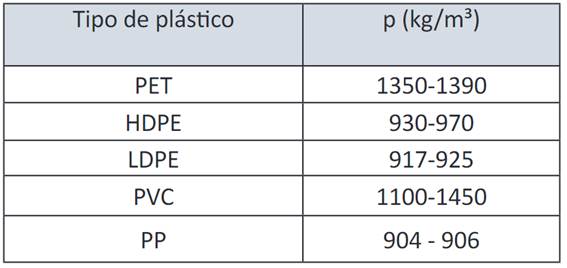
De acuerdo a los resultados detallados en la Tabla 3. en el Test de densidad, para considerar que una partícula no ha sufrido ningún cambio y/o reacción, la muestra no debe aumentar su tamaño ni debe disolverse con el agua 24. Considerando estos parámetros y atribuyendo a la muestra resultados favorables para el Test de densidad, se estipula que la muestra NO FLOTA. De acuerdo a la Tabla 1, la densidad del plástico a hidrolizar es superior a la densidad del agua (P plástico > 997 kg/m³ ) , descartando la posibilidad que el material corresponda a: LDPE, HDPE o PP 21.
En el test de Beilstein, se observó una llama naranja, es decir, una reacción negativa. De acuerdo a la teoría, el halógeno presente en los polímeros reacciona con el óxido de cobre (II) dando lugar a la formación de haluros de cobre (II) y al estar en presencia de calor, se forma la llama verde 25). El plástico PVC se elimina como una opción 20.
De igual manera, se rechaza la idea de la presencia de poliestireno (PS) con el Test de acetona, debido a que no se ha evidenciado una reacción o degradación del material. Sin embargo, se obtuvo una reacción positiva en la última prueba; H2SO4 reacciona con el plástico como resultado de la hidrólisis ácida 24. Por lo tanto, se confirma la presencia de PET en la muestra a hidrolizar.
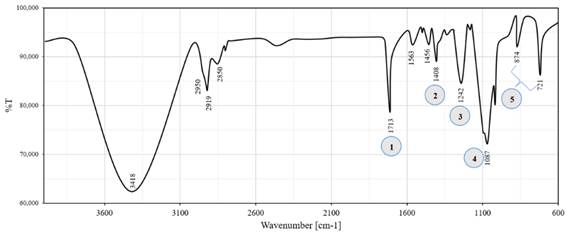
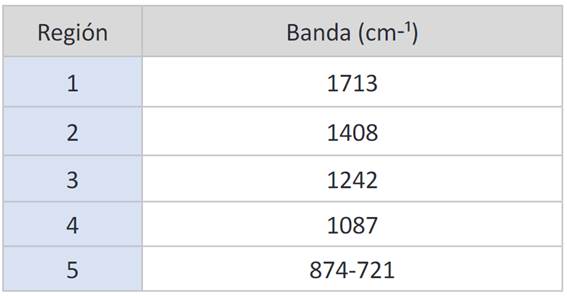
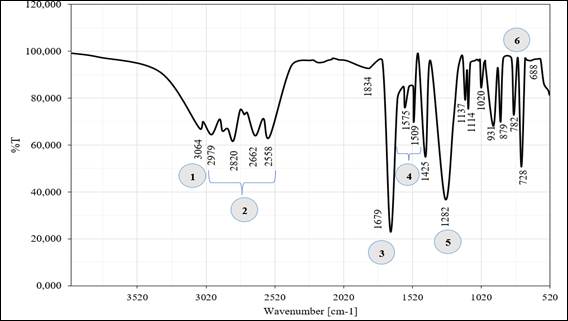
En la Figura 3, se aprecia el Espectro IR referente al PET. La banda 1, representan un estiramiento del carbonilo C = O atribuido a las vibraciones de los ésteres saturados 26. En la región 2 se aprecia un pico relacionado con la deformación asimétrica de CH2 - y segmentos de EG 27, con valores aproximados al trabajo de Silva et al. Además, 3 indica la presencia de la absorción específica de los enlaces del grupo tereftalato (OOC - C6H4 - COO). Estiramiento de los enlaces C-O se encuentran en la región 4.
Los dos picos de la zona 5, corresponden a la vibración =C-H del anillo de benceno. El espectro presentado efectivamente pertenece al PET, y está confirmado por el pico 721 cm-¹ 28, que es atípico para los aromáticos di-sustituidos (860-780) cm-¹ y se debe a la interacción del grupo éster polar y el anillo benceno.
Análisis infrarrojo de los pigmentos
Para la identificación de los pigmentos del plástico se recolectó la fracción sólida NO despolimerizada y se procedió con su análisis en el espectrofotómetro infrarrojo.
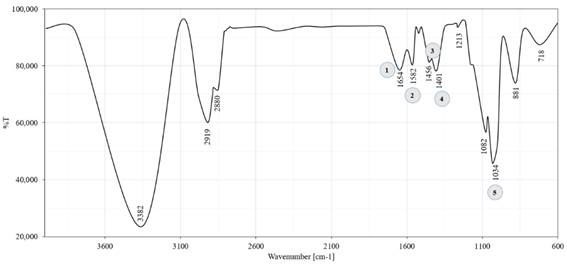
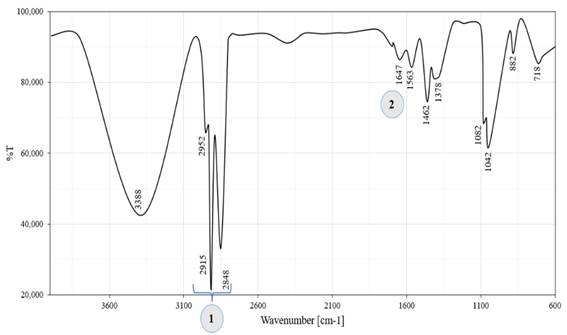
La Figura 5 perteneciente al pigmento verde. El espectro IR no detalla una banda pronunciada característica de la unión metal- oxígeno (M-O) en 668 cm-¹, por lo cual se descarta la presencia de pigmentos inorgánicos 29.
Entre los pigmentos verdes aptos para el uso en alimentos en encuentran las ftalocianinas (Fc) 30. Por lo tanto, la región 1 corresponde al estiramiento C=C. Las vibraciones del anillo de pirrol se encuentran en la banda 2. Los picos intermedios ubicados en 3 y 4 pertenecen al estiramiento C-C y C-N. Al pico 5 se atribuyen vibraciones C-H del anillo de Fc 31.
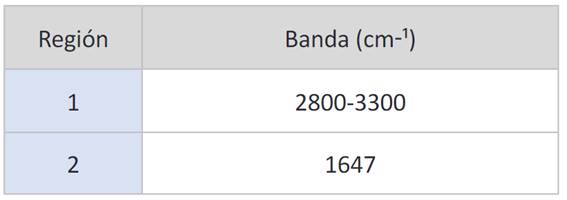
Por lo general, los pigmentos inorgánicos son óxidos metálicos 32. Tal como se indicó en la figura anterior, no se evidencia la presencia de una banda perteneciente al enlace entre M-O. Por ello, la Figura 6 no pertenece a un pigmento inorgánico. Sin embargo, la quinacridona (QA) es el pigmento orgánico comúnmente usado por la industria de los plásticos 33.
En la banda 1, se presenta bandas de absorción correspondientes a modos de estiramiento C-H y N-H de la QA 34. Además, para la banda 2 se asigna el estiramiento C=O del esqueleto de QA35 con un valor muy cercano al presentado en el trabajo de Imura et al.
Rendimiento
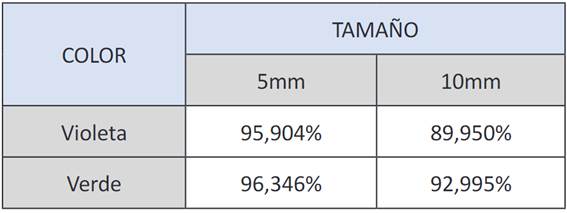
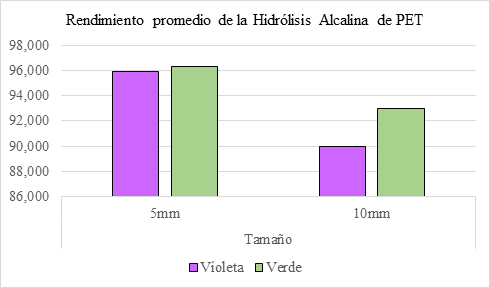
El rendimiento promedio de la reacción para cada color y tamaño de partícula se muestran en la Tabla 7.
Análisis Estadístico
Para el estudio estadístico se empleó un análisis Anova de dos factores, considerando las variables de clasificación: color, tamaño e interacción entre ellas, el rendimiento como la variable dependiente.
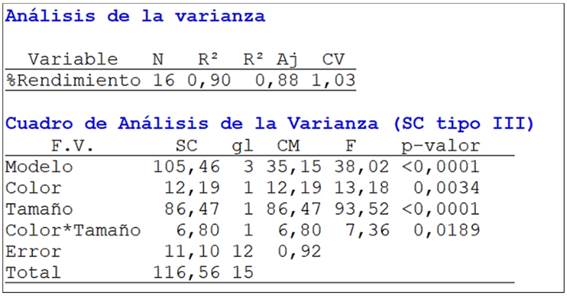
Para el análisis Anova detallado en la Figura 8, las tres condiciones establecidas para el modelo estadístico (color, tamaño e interacción) obtienen un valor R2 de 0,9. El p-valor de las tres variables es inferior a 0,05. Demostrando que sí existe diferencias estadísticamente significativas entre las dos variables incluida la interacción. Por lo cual, se acepta la hipótesis alterna (investigador) y se rechazan las hipótesis nulas. Al menos, una de las medias es distinta de cero.
Test Tukey
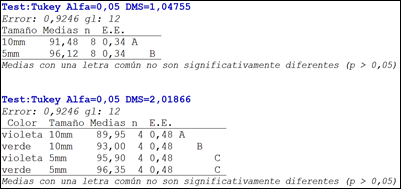
En la Figura 9 se aprecian diferencias significativas entre T5mm y T10mm. Además, en cuanto al cuadro correspondiente a la interacción de variables, entre los grupos: A, B y C también existen diferencias estadísticamente significativas. Sin embargo, entre violeta T5mm y verde T5mm no existe diferencia debido a que las medias registradas en el Test Tukey coinciden el grupo C.
En la Tabla 7 se describe el rendimiento promedio obtenido de la hidrólisis alcalina del PET. De acuerdo, a los resultados obtenidos en el análisis estadístico Anova y el test Tukey. Entre los factores que intervienen en el porcentaje de rendimiento se encuentra el color del plástico, así como el tamaño de partícula.
A medida que el tamaño del material disminuye, el rendimiento de la hidrólisis aumenta. En consecuencia, el rendimiento más bajo corresponde al plástico violeta T10mm con un valor de 89,950%. El mejor rendimiento es para plástico verde T5mm con porcentaje de 96.346%. Este fenómeno se debe a la velocidad de reacción de la hidrólisis alcalina es proporcional al área superficial de la partícula. En otras palabras, el plástico con un área superficial alta permite una reacción directa entre NaOH y el plástico PET 17.
De acuerdo al trabajo desarrollado por Fonseca et al. La hidrólisis alcalina con NaOH sigue el modelo de núcleo en contracción debido a que la reacción ocurre únicamente en la superficie externa de las partículas 36. A pesar de que se obtienen mejores rendimientos con tamaños de partícula bajos, se debe tener cuidado con los polvos debido a que son complicados de manejar. Sobre todo, en la actualidad la micronización de polímeros no es habitual en el campo industrial 19.
Los pigmentos orgánicos de las Figura 5 y Figura 6 han sido incorporados en los plásticos del estudio. Pigmentos orgánicos como: ftatocianina, antraquinona y quinacridona presentan carbonos electrofílicos en sus estructuras moleculares, lo que afecta y limita la posibilidad de un ataque directo por parte del hidróxido (nucleófilo) sobre los carbonos electrofílicos en la molécula de PET. Por lo tanto, estas especies químicas contribuyen a la reducción de la pureza del TPA, así como en el rendimiento 37.
Se puede llegar a considerar que los pigmentos presentes de estos plásticos actúan como un inhibidor, afectando de esta manera el porcentaje de rendimiento. También es importante señalar que, acorde a los resultados obtenidos en el análisis estadístico Anova y el test Tukey. Si se trabaja con aquellas interacciones en las que no se han presentado diferencias significativas, no se obtendrán porcentajes de rendimiento que difieran relativamente entre ellos.
Caracterización del ácido tereftálico
El ácido tereftálico es un compuesto químico que posee una solubilidad extremadamente baja y su reactividad es aún más lenta 38. Es por tanto que, en cuanto a la prueba de solubilidad, se observó que con los solventes orgánicos y con el agua destilada se dio la formación dos fases.
El ácido tereftálico es muy poco soluble en compuestos orgánicos y aumenta su solubilidad lentamente con el aumento de la temperatura. La solubilidad en agua a 25°C es de 0.0017gTPA/100g de solvente mientras que a 200°C es de 1,7 gTPA/100g de solvente 39. Los ácidos dicarboxílico no son líquidos a temperatura ambiente.
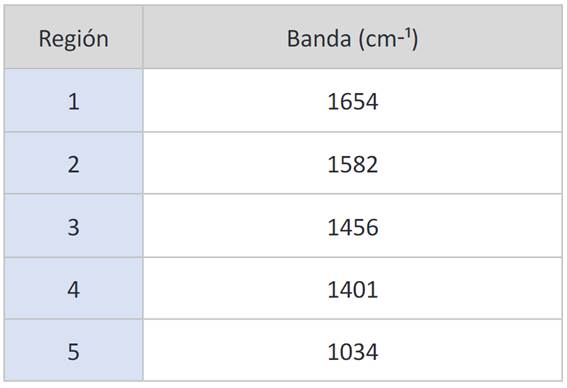
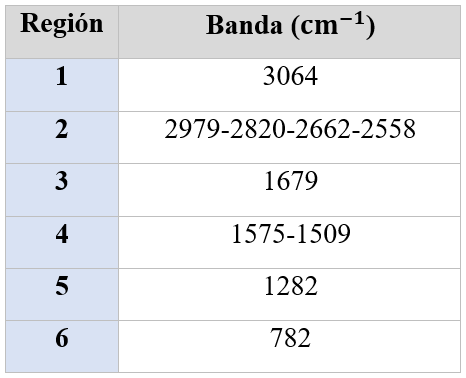
En la Figura 11 se detalla grupos funcionales característicos del TPA. La región 1, se evidencia un grupo aromático fuerte. De igual manera, un aromático es evidente en el pico 5. Se incorpora la zona 2 para las bandas -OH de ácidos carboxílicos. El pico inherente y característico TPA se observa en 3, con una banda de estiramiento C=O del carboxilo 40. La banda 4 simboliza una sustitución 1-4 correspondiente al anillo aromático 23, los cuales son valores próximos a los registrados en el estudio de Căta et al. Por último, la banda específica para anillos de benceno "para-sustituidos" se ubica en 6.
CONCLUSIONES
Para las dos pruebas de identificación del plástico, siguiendo el diagrama presentado en la presente investigación, se descartó cualquier tipo de plástico que no sea el tereftalato de polietileno. Con el test de Beilstein se apreció una llama naranja y la formación de un precipitado blanco con el ácido sulfúrico. Con en análisis IR, se encontró un pico muy representativo que se observa a 1242 cm-¹ el cual representa al grupo tereftalato.
El rendimiento máximo corresponde al plástico verde T5mm. El tamaño de partícula del plástico influye significativamente en el porcentaje de rendimiento de la hidrólisis alcalina. Para obtener mejores resultados es necesario trabajar con un tamaño mínimo, además de elegir preferentemente plásticos transparentes. Los resultados obtenidos, tanto por espectroscopia FT IR como por pruebas de solubilidad, mostraron que el producto final de despolimerización es el ácido tereftálico, siendo este uno de los principales monómeros del PET.