Forma sugerida de citar:
Reyna, S. y Arteaga, J. (2022). Riesgos de contaminación química en leche y sus derivados. La Granja: Revista de Ciencias de la Vida. Vol. 36(2):122-134. http://doi.org/10.17163/lgr.n36.2022.10
1 Introducción
La leche es un líquido blanco que segregan las mamas de las hembras de los mamíferos para alimento de sus crías (RAE, 2019). Con una producción estimada de 522 millones de toneladas métricas en el año 2019, la leche bovina es la más consumida por la población (85%), aunque en algunas regiones se registra un significativo consumo de leche de búfalo (11%) y de otros rumiantes (3,9%) (Kalyankar y col., 2016; STATISTA, 2020). En todas las latitudes los lácteos son susceptibles a contaminación química (OMS, 2018; Dimitrieska y col., 2016), que ocurre a través de los suelos, prácticas agrícolas, prácticas de producción lechera y durante su procesamiento (Nguyen y Flint, 2020; Priyanka, Sheoran y Ganguly, 2017), constituyendo un problema importante para la salud pública puesto que 1) varios de los agentes químicos son altamente estables, por lo que se incorporan a la cadena alimenticia incluso cuando su uso esté prohibido desde hace décadas, 2) no son susceptibles de disminuir tras la aplicación de tratamientos físicos, químicos o biológicos de la leche, contaminando por extensión a los derivados lácteos, 3) la naturaleza lipofílica de varios contaminantes determina un efecto acumulativo en el organismo animal y su presencia en la grasa de los lácteos 4) la exposición crónica a estos contaminantes tiene el potencial de deteriorar severamente la salud de la población (Akhtar y Ahad, 2017; Ismail y col., 2019). Por ello se revisará el conjunto de contaminantes de la leche y sus derivados en relación a sus características estructurales, en aspectos como su ingreso al organismo animal, a los mecanismos por los que ejercen efectos deletéreos sobre la salud, tras el consumo crónico de lácteos con concentraciones de agentes químicos en niveles superiores a los límites máximos de residuos (LMR) permitidos en leche bovina, y que se describen en la presente revisión. Finalmente, se señalan los principales métodos utilizados para su detección y se proponen estrategias para prevenir y controlar la contaminación química de los lácteos.
2 Contaminantes químicos
2.1 Aflatoxinas
Las aflatoxinas (AF) son micotoxinas ampliamente distribuidas que, tras contaminar los cultivos e ingresar en la cadena alimenticia, afectan la salud y productividad animal y la seguridad alimentaria de la población al presentar efectos tóxicos, mutagénicos, teratogénicos, carcinógenos e inmunosupresores (OMS, 2018; Dimitrieska y col., 2016; Ayar, Sert y Çon, 2007).
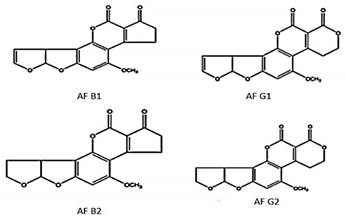
Aunque se han reportado más de veinte tipos de AF (Nguyen y Flint, 2020), AFB1, AFB2, AFG1 y AFG2 son las principales micotoxinas relacionadas con la contaminación de los lácteos. AFB1 y AFG1 difieren estructuralmente de AFB2 y AFG2 al disponer de un enlace doble adicional. Por otra parte, las AFG presentan un anillo de furano, mientras las AFB disponen de un anillo de lactona. En función de su grado de toxicidad y carcinogenicidad, resulta el siguiente orden: AFB1 > AFG1 > AFB2 > AFG2, cuyas estructuras se observan en la Figura 1 (AECOSAN, 2015).
La aflatoxina B1 (AFB1) es producida por hongos, particularmente Aspergillus flavus y Aspergillus parasiticus (Fels-Kler y Camenzuli, 2016; Duarte y col., 2013). A. flavus coloniza principalmente las partes aéreas de las plantas, encontrándose en alimentos almacenados como cacahuete, maíz, semillas de algodón y piensos. A. parasiticus se encuentra principalmente en el suelo y tiene una distribución similar a A. flavus, pero raramente se observa en el maíz (Van Asselt y col., 2016; IARC, 2002). Aunque la temperatura y la humedad son los principales factores que inciden sobre la presencia de AF en los alimentos, el transporte internacional de productos agrícolas determina que ninguna región del planeta está libre de ella (IARC, 2002).
En el tejido hepático de los rumiantes la AFB1 es metabolizada a aflatoxina M1 (AFM1), que es secretada en la orina, heces y leche, principalmente durante las 48 horas posteriores al consumo de alimentos contaminados, reduciéndose a niveles indetectables 96 horas después (Marchese y col., 2018; Nguyen y Flint, 2020). Las tasas de traspaso de AFB1 a AFM1 en leche se han estimado entre 0,3% a 6,2% (Vaz y col., 2020), siendo el maíz y otros alimentos concentrados contaminados las principales fuentes de AFM1 en la leche cruda (Fink, 2008), que a su vez es el principal introductor de esta aflatoxina en la dieta humana (Dimitrieska y col., 2016; Duarte y col., 2013; Vaz y col., 2020). AFM1 apenas es afectada por la pasteurización (Neagu y col., 2009), encontrándose en la leche pasteurizada (Van Asselt y col., 2016), ultra pasteurizada (UHT) (Duarte y col., 2013), quesos (Urbán y col., 2009) y yogur (Rahimirad y col., 2014).
Aunque no se ha especificado una Ingesta Diaria Tolerable (IDT) para las AFM1, la Unión Europea ha establecido su LMR en 0,05 µg/L para leche cruda, leche pasteurizada y leche utilizada en la elaboración de productos lácteos, y en 0,025 µg/L para fórmulas y alimentos dietéticos para infantes; mientras que en Estados Unidos, China y Brasil el LMR para AFM1 en leche es 0,5 µg/L. A pesar de que los niveles máximos de AF están regulados en más de 80 países, no existe armonización internacional al respecto (Nguyen y Flint, 2020; Akbar y col., 2019; Vaz y col., 2020; Rahimirad y col., 2014).
Debido a la estabilidad, toxicidad y los LMR permitidos para las AF, y en particular AFM1, su cuantificación es extremadamente importante. En este sentido, el ensayo por inmunoabsorción ligado a enzimas (ELISA) se utiliza comúnmente con fines de cribado, mientras que la cromatografía líquida de alto rendimiento (HPLC) con detección por fluorescencia o espectroscopía de masas se emplea frecuentemente para la identificación y cuantificación de AF en alimentos y piensos (Vaz y col., 2020; Rahimirad y col., 2014).
Para reducir la contaminación fúngica y la producción de AF en los alimentos se ha planteado la rotación de cultivos, la prevención de infestaciones y el deterioro de granos, el uso de variedades de semillas resistentes, cosechas con bajos niveles de humedad, la promoción de la deshidratación, el almacenamiento y el transporte adecuado de granos y el monitoreo de AF en los piensos (Van Asselt y col., 2016; IARC, 2002). Aunque es imposible prevenir completamente la contaminación de la leche (Ayar, Sert y Çon, 2007), limitar el acceso del ganado lechero a alimentos con altas concentraciones de AFB1 contribuye a evitar la contaminación láctea (Dimitrieska y col., 2016; Ayar, Sert y Çon, 2007). Por otra parte, la aplicación de métodos físicos, químicos y biológicos como alternativas para reducir el contenido de AFM1 en leche es cuestionable y representa un riesgo adicional para la seguridad alimentaria (Nguyen y Flint, 2020; Rahimirad y col., 2014).
2.2 Residuos de fármacos veterinarios
Antibióticos
Los antibióticos son utilizados desde el siglo anterior como promotores de crecimiento animal y en la prevención y tratamientos de enfermedades (Albright, Tuckey y Woods, 1961; Sachi y col., 2019). El incumplimiento de los tiempos de retiro de la leche, el uso de antibióticos fuera de las prescripciones, su empleo como aditivos alimentarios y un limitado o inexistente sistema de monitoreo, entre otros factores, determinan LMR de residuos de antibióticos (RA) superiores a los legalmente establecidos, lo que representa una seria amenaza para la salud pública, especialmente de grupos etarios vulnerables, y contribuye a la aparición de la resistencia microbiana (Priyanka, Sheoran y Ganguly, 2017; Albright, Tuckey y Woods, 1961; Kurjogi y col., 2019; Sachi y col., 2019). Para la detección de RA en leche se utilizan métodos de tamizaje y confirmatorios; los primeros incluyen ensayos de inhibición de crecimiento bacteriano, ensayos enzimáticos de unión a receptores e inmunoensayos (Navrátilová, 2008; Padol y col., 2015), mientras que las pruebas cromatográficas tienen carácter confirmatorio, ofreciendo mayor sensibilidad, especificidad y cuantificación del analito (Priyanka, Sheoran y Ganguly, 2017; Sachi y col., 2019).
Como medidas para reducir la concentración de RA en los lácteos se ha propuesto la educación del productor lechero, el cumplimiento estricto del tiempo de retiro (Albright, Tuckey y Woods, 1961), el uso de técnicas adecuadas para la detección de RA en lácteos (Priyanka, Sheoran y Ganguly, 2017; Sachi y col., 2019), la supresión de antibióticos como promotores de crecimiento, la adopción de prácticas de manejo e higiene durante el ordeño y procesado de la leche y la reducción al mínimo del uso de antibióticos o su sustitución por probióticos, inmunomoduladores, ácidos orgánicos y suplementos alimenticios (Priyanka, Sheoran y Ganguly, 2017; Sachi y col., 2019; Padol y col., 2015; Yang y col., 2019).
Antihelmínticos
Los antihelmínticos se utilizan para tratar parasitosis de gusanos planos (tenias y tremátodos) y gusanos redondos (nemátodos). En función de su estructura química y modo de acción, se clasifican principalmente en benzimidazoles (albendazol, fenbendazol, flubendazol, mebendazol, oxfendazol, tiabendazol, triclabendazol), tetrahidropirimidinas (levamisol, pirantel, morantel), imidazoles (tetramisol, levamisol) y lactonas macrocíclicas (abamectina, doramectina, ivermectina, selamectina, moxidectina) (Romero-González, Frenich y Vidal, 2014).
El uso incorrecto de antihelmínticos contribuye a su ingreso en la cadena alimenticia, observándose sus residuos en la leche (Romero-González, Frenich y Vidal, 2014; Cerqueira y col., 2014). En este alimento, la concentración de benzimidazoles no es afectada por la cocción, el almacenamiento a bajas temperaturas (−18 ◦C), el horneado o la acción de microondas (Tsiboukis y col., 2013), mientras que los residuos de levamisol son estables durante los procesos de fermentación y el tratamiento térmico del suero, persistiendo en quesos (Whelan y col., 2010). Frente al tratamiento térmico, las lactonas macrocíclicas presentes en la leche son parcialmente degradadas, lo que no sucede cuando están presentes en la crema de leche (Avcı y Filazi, 2020).
En varias especies, los benzimidazoles se han asociado con efectos carcinogénicos, genotóxicos, embriotóxicos y teratogénicos (Romero-González, Frenich y Vidal, 2014; Tsiboukis y col., 2013; Santos y col., 2019), mientras que la ivermectina presenta efectos mutagénicos y teratogénicos en varios mamíferos, además de un efecto ecotóxico (Santos y col., 2019; Pérez-Cogollo y col., 2018). Así, los residuos de antihelmínticos en los alimentos implican un riesgo para la salud pública (Padol y col., 2015; Romero-González, Frenich y Vidal, 2014; Avcı y Filazi, 2020). En la Tabla 1 se aprecian los LMRs permitidos de varios antihelmínticos y antibióticos en leche bovina. Por otra parte, el seguimiento de las prescripciones veterinarias, la observancia de periodos de retiro en la producción láctea tras la aplicación de los antihelmínticos y el control y monitoreo de residuos de antiparasitarios contribuyen a prevenir su contaminación. Los métodos cromatográficos son los más utilizados para identificar y confirmar la presencia de antihelmínticos en la leche (Cerqueira y col., 2014; Santos y col., 2019).
Pesticidas organoclorados y organofosforados
Los pesticidas son “compuestos químicos destinados a prevenir, destruir, atraer, repeler o controlar cualquier plaga, incluidas las especies no deseadas de plantas o animales durante la producción, almacenamiento, transporte y procesamiento de alimentos, productos agrícolas o alimentos para animales o que pueden ser administrados a animales para el control de ectoparásitos” (FAO/OMS, 2013).
En función de su capacidad de incorporarse a la cadena alimenticia, de bioacumulación y toxicidad, los pesticidas organoclorados (POC) y organofosforados (POF) destacan como contaminantes de la leche y sus derivados, que, a pesar de su progresiva prohibición, aún constituyen un riesgo para la salud pública.
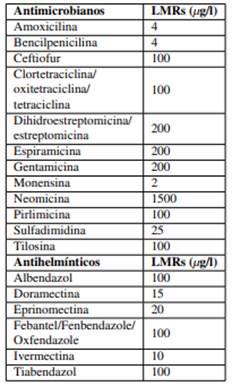
Tabla 1. Límite Máximo de Residuos (LMRs) para antimicrobianos y antihelmínticos en leche bovina (FAO/OMS, 2008).
Los POC o hidrocarburos clorados son compuestos químicos sintéticos de amplio espectro que incluyen a los derivados de los etanos, como el diclorodifeniltricloroetano (DDT), ciclodienos, entre ellos clordano, aldrin, dieldrin heptacloro, endrín y toxafeno, y los hexaclorociclohexanos (HCH) como el lindano (Zaragoza-Bastida y col., 2016).
Las principales rutas de contaminación por POC incluyen inadecuadas prácticas de manejo, como el almacenaje de pesticidas junto a alimentos, la fumigación de cosechas en áreas adyacentes a las granjas lecheras, provocando la deposición de pesticidas en el agua y alimentos (Bedi y col., 2018), la transmisión transcutánea, la fertilización del suelo con lodos residuales y la utilización de alimento animal procedente de países en los que aún se utiliza lindano y DDT (Rusu y col., 2016; Fischer y col., 2016). La elevada estabilidad en el ambiente y liposolubilidad determinan la deposición de los POC en tejidos animales particularmente ricos en grasas y en la leche (Zaragoza-Bastida y col., 2016; Rusu y col., 2016), siendo considerados como un contaminante orgánico persistente (COP) (OMS, 2020). La movilización del tejido adiposo para mantener la secreción láctea, particularmente en ganadería basada en el pastoreo o en caso de desnutrición del ganado, implica que la leche de estos animales registre un incremento en la concentración de estos pesticidas (Fischer y col., 2016).
A pesar de reportarse concentraciones decrecientes de POC y sus derivados en relación a estudios precedentes, debido probablemente a que estos compuestos fueron prohibidos décadas atrás, aún se informa en distintas regiones del mundo de contaminación por POC, ocasionalmente superando los LMR establecidos en leche cruda, leche pasteurizada, crema agria, queso y mantequilla. Así, los humanos están expuestos a estos contaminantes principalmente a través de alimentos de origen animal (Akhtar y Ahad, 2017; Ishaq y Nawaz, 2018; Rusu y col., 2016), constituyendo una amenaza para la salud pública debido a sus efectos mutagénicos, teratogénicos y deletéreos sobre los sistemas endocrino, cardiovascular y respiratorio. Adicionalmente, varios pesticidas organoclorados como DDT, HCH y hexaclorobenceno (HCB) son posibles cancerígenos para el ser humano (Rusu y col., 2016).
Por otra parte, al presentar menor estabilidad y persistencia, los pesticidas organofosforados (POF) como diclorvos, diazinón, dimetoato, clorpirifos, malatión y metilparatión han reemplazado a los POC. Así, ingresan al organismo animal a través de alimentos y aguas contaminadas, bien por inhalación, por el uso de insecticidas en pasturas, establos y factorías lecheras, o a través de la piel intacta tras la aplicación de ectoparasiticidas y posterior violación del periodo de retiro establecido (Bedi y col., 2018; Fischer y col., 2016; Fernández, Mancipe y Fernández, 2010). La naturaleza lipofílica y su capacidad para unirse covalentemente a las proteínas determinan la presencia de POF en la leche y su posterior incorporación a la cadena alimenticia, detectándose en leche pasteurizada, leche cruda y quesos (Salas y col., 2003; Al-Julaifi y col., 2015; Pagliuca y col., 2006). Los POF tienen potenciales efectos sobre la salud humana y animal, ocasionando la estimulación excesiva de los receptores de acetilcolina y con ello debilidad o parálisis muscular, excesiva actividad secretora y cambios en el estado de conciencia (Bedi y col., 2018; Fernández, Mancipe y Fernández, 2010). En la Tabla 2 se exponen los LMR en leche para varios pesticidas organoclorados y organofosforados.
Se ha planteado que el control de la polución ambiental en las explotaciones lecheras (Bedi y col., 2018), el mejoramiento de las condiciones de almacenamiento de los alimentos destinados al ganado lechero, los programas de educación a granjeros, el control de ventas de pesticidas, la aplicación de agricultura orgánica, la implementación de métodos de manejo integrados de pastos (Rusu y col., 2016), la identificación de fuentes de contaminación, el monitoreo de residuos de pesticidas en el alimento animal y en lácteos mediante cromatografía de gases (GC), cromatografía líquida/ espectrometría de masas (LC/MS) y cromatografía líquida acoplada a espectrómetros de masas en tándem (LC/MS/MS) (Akhtar y Ahad, 2017) pueden contribuir a reducir la presencia de estos pesticidas en la leche y sus derivados.
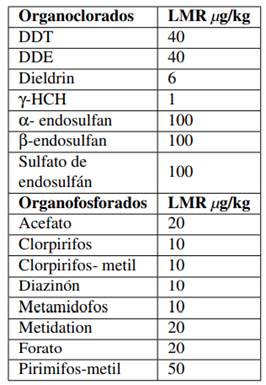
Tabla 2. LMRs para varios organoclorados y organofosforados (Ishaq y Nawaz, 2018; Pagliuca y col., 2006).
2.3 Metales pesados
Son elementos metálicos y metaloides, con una densidad mayor en comparación a otros elementos metálicos (5 g/cm3 o un peso atómico entre 63,5-200,6 g/mol), se encuentran ampliamente distribuidos en el ambiente e inducen a toxicidad sistémica incluso en bajos niveles de exposición (Ismail y col., 2019; Mahmoudi y col., 2017; Jan y col., 2015). Aunque en este grupo se han considerado al hierro (Fe), zinc (Zn), níquel (Ni) y cobre (Cu) cuando se encuentran en productos alimenticios más allá de ciertos límites, los metales pesados más tóxicos hallados en los alimentos generalmente son mercurio (Hg), arsénico (As), cadmio (Cd) y plomo (Pb). Acorde a las ediciones de la Comisión del Códex Alimentarius de 2011 y 1999, se ha establecido el nivel máximo permitido de Pb y Cd en leche en 0,02 µg/ml y 0,01 µg/ml, respectivamente. La Unión Europea ha establecido en 0,1 µg/ml el nivel máximo permitido para As, en tanto que la legislación hindú estipula en 1,0 µg/ml como los límites máximos permisibles de mercurio en la leche y productos lácteos (Ismail y col., 2019).
Actividades antropogénicas como la urbanización, la industrialización, el riego con agua contaminada, la aplicación de fertilizantes que contienen metales pesados y condiciones no higiénicas en el procesamiento y distribución de la leche determinan su ingreso al organismo, reportándose en muestras de leche cruda, pasteurizada y en polvo (Ismail y col., 2019; Mahmoudi y col., 2017; Jan y col., 2015). La contaminación de la leche y sus derivados con metales pesados es importante para la salud pública, porque ocasionan lesiones y enfermedades especialmente en infantes y ancianos, quienes son los principales consumidores de lácteos (Ismail y col., 2019; Mahmoudi y col., 2017). Así, una de las principales causas del saturnismo o plumbosis es justamente el consumo de leche contaminada con plomo, cuya tasa de absorción en niños es 40% mayor que en los adultos (Ismail y col., 2019; Harlia, Rahmah y Suryanto, 2018). Desde el punto de vista fisiopatológico, los metales estimulan la generación de especies reactivas de oxígeno y nitrógeno, generando estrés oxidativo y deteriorando el sistema antioxidante celular (Jan y col., 2015).
Entre los métodos utilizados para detectar metales pesados en lácteos se menciona la electroforesis capilar, voltamperometría de pulso y métodos espectrométricos. Para prevenir el ingreso de estos elementos en la cadena alimenticia se ha propuesto reducir sus concentraciones en el agua destinada a vacas lecheras, utilizando agentes adsorbentes como esmectita, paligorskita y zeolita, así como el monitoreo del alimento, el uso de materiales inocuos para el procesamiento y envasado de lácteos, el análisis periódico de estos productos y el monitoreo del agua utilizada en el procesamiento de la leche y productos lácteos (Mahmoudi y col., 2017). Adicionalmente, el suministro de comino (Cuminum cyminum L.), cúrcuma blanca (Curcuma zedoaria Rosc.) y cúrcuma amada (Curcuma mangga Val.) en el alimento de vacas lecheras reduce la concentración de plomo en la leche y la incrementa en las heces, probablemente al modular el microbiota ruminal (Nurdin, Putra y Amelia, 2013). Así mismo, se ha observado una menor concentración de metales pesados en el yogur en comparación con la leche cruda, efecto atribuido a procesos de fermentación, como consecuencia de la actividad bacteriana (Enb y col., 2009).
2.4 Dioxinas y bifenilos policlorados análogos a las dioxinas (PCB-AD)
Son un grupo de compuestos policlorados, casi aromáticos planares con estructuras físicas y químicas similares, constituidos por 75 congéneres de policlorodibenzo-p-dioxinas (PCDD) y 135 policlorodibenzofuranos (PCDF). De las dioxinas (PCDD/Fs), 17 presentan propiedades toxicológicas y 12 de los 209 bifenilos policlorados (PCB); al adoptar una estructura planar análoga a las dioxinas presentan propiedades toxicológicas similares a éstas (análogos a las dioxinas, PCB-AD) (DO, 2011; AECOSAN, 2018).
Estos compuestos se caracterizan por ser altamente estables en el medio por su ubicuidad, por su toxicidad y su capacidad de ingresar al organismo a través del aire, suelo o sedimentos, mediante inhalación, absorción cutánea y especialmente por la ingesta de alimentos contaminados (AECOSAN, 2018; Gallego y col., 2005). En rumiantes, la ingesta de PCDD/Fs y PCB-AD ocurre principalmente durante el pastoreo, por el consumo de pasto contaminado y partículas de suelo, así como por el consumo de ensilados y forrajes sometidos a procesos de secado (Bogdal y col., 2017).
Una vez acumulados en el organismo, principalmente en el tejido adiposo animal, la gestación y lactancia significarán la movilización de estos compuestos, incrementando su concentración en la leche que, junto a sus derivados, se convierte en una potencial fuente de dioxinas y PCB-AD para el consumidor (Gallego y col., 2005; Schulz y col., 2005; Piskorska-Pliszczynska y col., 2017). Se han detectado dioxinas en más del 90% de las muestras de fórmulas infantiles, de mantequillas y otros productos lácteos (yogur, postres lácteos congelados, productos horneados que contienen lácteos) y diversos tipos de quesos (CFIA, 2019), planteando una seria amenaza para la salud pública. Las PCDD/Fs y PBC-AD presentan efectos cancerígenos, teratogénicos, y mutagénicos, y se asocian con alteraciones dérmicas y hemáticas que actúan como un disruptor endocrino causante de alteraciones reproductivas, inmunológicas y neurológicas (Gallego y col., 2005).
Para prevenir que los alimentos destinados a animales productores de leche sean contaminados por dioxinas y PCB-AD, se ha planteado la identificación de zonas agrícolas con importante presencia de estos compuestos, la identificación y seguimiento de piensos e ingredientes de piensos originarios de estas zonas, el monitoreo de la concentración de dioxinas y PCB-AD en fangos cloacales y compost utilizados en agricultura, y la identificación y control de procesos críticos de fabricación de piensos (por el ejemplo el secado artificial mediante calentamiento directo) (FAO/OMS, 2018). También se puede prevenir la ingesta de partículas del suelo contaminado por dioxinas y PCB al reducir la densidad animal durante el pastoreo y al incrementar la disponibilidad de pasturas. Debido a que las dioxinas permanecen en el organismo animal durante 30 a 60 días antes de ser excretadas a través de la leche, se ha propuesto la transferencia de animales a suelos no contaminados por un periodo de tres meses, a fin de reducir su contenido en la leche. Puesto que se ha reportado contaminación láctea con PCB-AD tras la ingesta de restos de pinturas en establos y el pastoreo en zonas cercanas a centros industriales, estas deben considerarse como potenciales fuentes de contaminación (Gallego y col., 2005; Bogdal y col., 2017; Schulz y col., 2005).
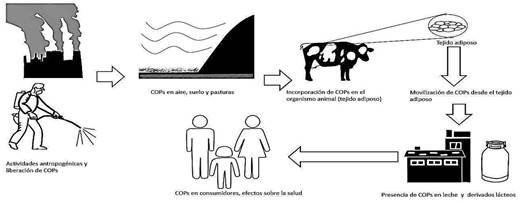
Los PCDD/Fs y los PCB-AD, junto con los pesticidas organoclorados, son los contaminantes orgánicos persistentes (COPs) más frecuentes (OMS, 2020), que son liberados en el ambiente como consecuencia de diversas actividades antropogénicas e ingresan a la cadena alimentaria debido a su capacidad de transporte, toxicidad y persistencia (Figura 2).
La detección de las PCDD/Fs y PCB-AD se basa en la cromatografía de gases junto con la espectrometría de masas de alta resolución (GC-HMRS). También se utilizan métodos basados en la cromatografía de gases junto con la espectrometría de masas en tándem (GC-MS/MS). Alternativamente se han desarrollado técnicas de bioensayo como métodos de cribado de alto rendimiento (FAO/OMS, 2018).
2.5 Desinfectantes y detergentes
La limpieza y desinfección son pasos críticos en la producción primaria y en el procesamiento posterior de lácteos, permitiendo eliminar restos de leche y minimizando el nivel de contaminación bacteriana en las instalaciones de ordeño. Para ello se emplean detergentes que incluyen tensioactivos en su composición y de desinfectantes, disponiendo de una amplia gama de productos que contienen biocidas como cloro, yodo, amonio cuaternarios y dióxido de cloro (Van Asselt y col., 2016; Fischer y col., 2016; Kirsanov y col., 2020). Si los procedimientos de lavado y desinfección en las vacas lecheras, así como el lavado y enjuague de los equipos de ordeño y almacenamiento de la leche se realizan incorrectamente, los residuos de detergentes y desinfectantes contaminan esa leche y sus derivados (Fischer y col., 2016; Merin y col., 1985; Šalomskiene˙ y col., 2013; Siobhan y col., 2012). Así, los equipos y utensilios utilizados en el procesamiento de la leche deben limpiarse, desinfectarse y enjuagarse con agua potable (a menos que las instrucciones del fabricante indiquen lo contrario) para posteriormente escurrirse y secarse (FAO, 2004).
Aunque los residuos de cloro en la leche se degradan rápidamente sin representar un riesgo para la salud (Fischer y col., 2016; Šalomskiene y col., 2013), el contacto del cloro con materia orgánica da lugar a que la leche presente residuos de contaminantes no añadidos intencionalmente, como el triclorometano (TCM) o cloroformo (Siobhan y col., 2012). Otros desinfectantes como dióxido de cloro generan subproductos cuya ingesta inhibe la absorción de yodo (Van Asselt y col., 2016), mientras que los amonios cuaternarios son estables en la leche, afectando negativamente la salud de los consumidores e inhibiendo los procesos de fermentación láctea y de elaboración de quesos (Siobhan y col., 2012). El LMR de desinfectantes y detergentes en leche y otros alimentos se ha estimado en 0,1 mg/kg (DO, 2014). Por otra parte, la elevada ingesta de yodo a partir de sus residuos en la leche puede conducir a desórdenes en la función de la glándula tiroides, principalmente en niños (Fischer y col., 2016).
Debido a la amplia variedad de productos desinfectantes, se han descrito varias técnicas analíticas para su detección en alimentos, incluyendo pruebas colorimétricas simples, potenciómetro con electrodos selectivos de iones, cromatografía de capa fina y cromatografía líquida y gaseosa. Para la cuantificación y detección de cloratos, percloratos y amonio cuaternarios en leche y productos lácteos se emplea la cromatografía - espectrometría de masas en tándem (Fischer y col., 2016).
3 Conclusiones
La leche es una fuente de nutrientes para un amplio sector de la población. Sin embargo, las actividades antropogénicas tendentes a mejorar la productividad animal y el procesamiento de lácteos ocasionan un riesgo de contaminación química de estos productos. Debido a la ubicuidad de estos contaminantes y sus efectos deletéreos tras su ingesta crónica a través de la leche y derivados lácteos, se han establecido Límites Máximos Residuales para la mayoría de estos compuestos, siendo necesario prevenir, o al menos minimizar, y monitorear la concentración de contaminantes químicos de lácteos, utilizando técnicas adecuadas de detección, contribuyendo a la seguridad alimentaria de la población.