INTRODUCIÓN
La enfermedad de Alzheimer (EA), es la forma más común de demencia contribuyendo con un 60-70% al total de casos.(1) Actualmente con el desarrollo de los biomarcadores de EA a través de la Resonancia Magnética (RM), el líquido cefalorraquídeo (LCR) y la Tomografía por emisión de positrones o PET (del inglés Positron Emission Tomography), ha favorecido el diagnóstico temprano y aun el pre-sintomático(2). En la fase prodrómica a la EA, se evidencia un deterioro cognitivo leve (DCL), en ocasiones con pérdidas de la memoria reciente y a veces con fallas en otras funciones cognitivas (3)(4)(5). Petersen y cols(6) describieron 4 tipos de DCL: 1. dominio único amnésico puro, 2. multidominio amnésico, 3. dominio único no amnésico y 4. multidominio no amnésico.
La batería neuropsicológica UDS (del inglés Uniform Data Set) (https://www.alz.washington.edu/WEB/forms_uds.html) tiene sus orígenes en 1984 cuando el Instituto Nacional de Envejecimiento (NIA del inglés National Institute on Aging) y el Instituto Nacional de la Salud (NIH del inglés National Intitutes of Health) ambos de EEUU crean 29 centros de Alzheimer (ADCs del inglés Alzheimer’s Disease Centers), y establecen una base de datos denominada CERAD (del inglés Consortium to Establish a Registry for Alzheimer’s Disease) con el fin de registrar y homogeneizar los resultados de las evaluaciones. Más tarde en 1997 se crea un comité entre ADCs y NIA, para definir datos neuropsicológicos comunes mínimos.
El centro nacional de coordinación de Alzheimer´s (NACC) promueve los estudios cooperativos entre estos centros (ADCs, del inglés Alzheimer's Disease Cooperative Study) tendiente a desarrollar un fenotipo de tipo comportamental, funcional y médico. Es entonces, cuando identifican la necesidad de generar uniformidad para mejorar la evaluación y el diagnóstico(7). A partir de allí en el 2002 designan un equipo directivo de cinco miembros de la NIA y siete miembros no votantes (2 de la NIA, 1 ADCs y 4 NACC) que crea el set de datos uniformes UDS (del inglés Uniform Data Set), con el fin de apoyar las nuevas investigaciones en enfermedad de Alzheimer. En el año 2004 se define y se adapta el UDS 1 donde se realiza la normalización para médicos y neuropsicólogos. Se toman datos transversales para evaluar su potencialidad en un estudio piloto. Es recién en el año 2006 donde se administran los datos y se le brinda acceso al público. En el año 2009 Weintraub y colaboradores,(8) publican la primera descripción de datos normativos, donde exponen el diseño del UDS y se evalúan las funciones atencionales, la velocidad del procesamiento, las funciones ejecutivas, la memoria episódica y el lenguaje. El mismo fue aplicado a 3,268 pacientes normales 85% de ellos eran blancos no hispanos en una relación 2:1 mujeres-hombres. Posteriormente fueron apareciendo las nuevas versiones el UDS 1.1 y UDS 1.2.
Morris y colaboradores(9) afirman que está bateria uniforme favorece los datos de investigación, ya que identifica riesgo de demencia, DCL y progresión del EA, y reportan en angloparlantes una sensibilidad del 71% para DTA. Sin embargo, rapidamente se evidenció la necesidad de una equivalencia cultural y lingüística en espanol a la versión en inglés.(10) Pero, con el paso del tiempo los síntomas prodrómicos comenzaron a generar mucho más interés, así que Teng y cols 2010,(11) sostienen que la UDS version 2 muestra una excelente validez en memoria, atención y lenguaje en la población con DCL, reflejando una baja consistencia interna para funciones ejecutivas y velocidad del procesamiento. A pesar de lo anterior, se ha reportado su utilidad en la práctica clínica en patologías neurodegerativas e incluso rangos descriptores entre el funcionamiento cognitivo normal y la demencia(12)
Actualmente, con apoyo del Instituto Nacional sobre el Envejecimiento (NIA), se han generado investigaciones que facilten el uso de la batería UDS, tal como la creación de una calculadora en línea (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3308021/) basada en regresión, que favorece la interpretación de los puntajes individuales de la UDS.(13) Incluso se reportan aplicaciones para implementar la regresión de cuartiles para las normas de referencia.(14)
A pesar del buen comportamiento de la UDS en su V.2, debido a los problemas de patentes de los test neuropsicologicos, en el 2015 se desarrolló una nueva batería de pruebas neuropsicológicas que sustituyeron con instrumentos equivalentes pero libres de patentes creando la UDS 3. Monsell y cols(15), muestran que este proyecto de “cross-walk” entre el UDS-2 y el UDS-3 tiene una correlación "buena" a "muy buena" con las pruebas anteriores, evidenciando intervalos de confianza razonablemente ajustados. Recientemente Weintraub y cols.(16) reportan el rendimiento en población normal de la base de NACC y sustenta que esta batería es sensible para DCL, así como que la edad y la educación son proporcionales en la puntuación.
Por lo anterior, la presente investigación tuvo como objetivo sintetizar cuantitativamente los resultados de las subpruebas de la UDS, para generar puntuaciones mediales, que funcionen como puntos de corte homogéneos para diferenciar demencia tipo alzheimer (DTA), deterioro cognitivo leve (DCL) y controles cognitivamente normales.
MATERIAL Y MÉTODO
Estrategia de búsqueda para la revisión sistemática
Se desarrolló una base de datos de artículos originales, a partir de búsquedas sistemáticas de fuentes electrónicas y búsqueda manual. Se realizaron búsquedas en las siguientes bases de datos: PubMed/ MedLine, Web Of Science(WOS), Scopus, Lilacs, Science Direct, Cochrane Library, PsycINFO. Se identificaron todos los estudios publicados desde 1984 hasta el 31 de enero 2018 que evaluaron la batería neuropsicológica UDS (Uniform Data Set) para detectar demencia de tipo Alzheimer y deterioro cognitivo leve. La búsqueda se limitó a la literatura en inglés y en español, no se incluyeron otros idiomas. Con el uso de operadores booleana de intercesión (AND e Y) y de suma lógica (O y OR) se realizó una búsqueda cruzada de las siguientes cuatro cadenas: 1. Batería neuropsicológica (“Uniform Data Set Neuropsychological Battery” OR “Uniform Data Set” OR “UDS” OR “Batería de datos Uniformes”) 2. Enfermedad (“Enfermedad de Alzheimer” OR “deterioro cognitivo leve”; “Alzheimer” OR “mild cognitive impairment”) 3. Aspectos psicométricos de la batería ("sensibility" OR " Specificity " OR "Accuracy"; “sensibilidad” OR “Especificidad” OR “Precisión”) y términos que representan pruebas de detección ("detection" OR “early detection”; “detección” OR “detección temprana”).
Criterios de inclusión y Selección de artículos
Para ser incluidos en la revisión los estudios tuvieron que cumplir los siguientes criterios: [1] Participantes: pacientes con demencia de tipo Alzheimer y/o deterioro cognitivo leve, pacientes en cualquier fase de enfermedad de Alzheimer (EA), sujetos normales (Controles). [2] Datos psicométricos: valores de sensibilidad (Sn) y especificidad (Sp) o el descrito del rendimiento promedio en cada subtest (Uso completo de la batería). [3] Resultados: precisión diagnóstica del UDS. [4] Tipo de estudio: artículos de investigación (métodos cuasi-experimentales o experimentales), excluyendo artículos de revisiones, teóricos o estudios de caso único y los metaanálisis.
Síntesis cuantitativa de las subpruebas para generar puntos de corte homogéneos.
De los estudios incluidos, los principales resultados de interés fueron las comparaciones mediales de los descriptivos de los subtest en estudios homogéneos, de los cuales se dividieron de acuerdo a los datos suministrados en los estudios con respecto a la puntuación directa o puntuación Z, utilizando el programa SPSS V.25. No se centró en significancia (Sn) y Especificidad (Sp), ya que únicamente es reportado en uno de los estudios con la batería UDS, por lo cual se incluyó dentro de la síntesis cualitativa. Se sintetizaron los resultados para el rendimiento de la prueba en población: [1] normal, [2] demencia tipo Alzheimer; y [3] deterioro cognitivo leve (DCL). Se siguió la declaración PRISMA17 para informar los ítems de esta revisión sistemática.
RESULTADOS
Búsqueda de literatura
La búsqueda sistemática cruzada con cuatro categorías arrojó tres mil setecientos treinta y nueve (3739) artículos, de los cuales treinta y tres (33) eran potencialmente relevantes. Con respecto, a los artículos incluidos en la comparación de medias de las sub-pruebas, todos son artículos originales, siete de ellos con un alcance descriptivos; con una temporalidad transversal,8 con análisis descriptivos-comparativos, (18)(19) con regresiones lineales, de acuerdo al rendimiento,(20)(21) con regresión logística polinómica.(22) Seis de ellos realizaron estudios longitudinales; con regresión logística descriptiva(23)(24) y con regresión logística con análisis predictivo o retrospectivo.(25)(26)(27)
Criterios de diagnóstico
Los datos fueron recolectados de la base de datos NACC, que contiene información clínica y neuropsicológica en las visitas iniciales a los centros de Alzheimer de Estados Unidos (ADC´s). Los estudios, cumplieron con los criterios establecidos en la evaluación inicial por el Estadio Clínico de Demencia (CDR del inglés Clinical Dementia Rating)(28) y los criterios de Petersen para DCL, 6)(29) ambos por consenso médico tipo panel de expertos. Los estudios que utilizaron población normal refirieron la evaluación neuropsicológica que los clasificaba como grupo control sano. Dentro del análisis, se utilizó un estudio realizado en la Republica Checa, el cual utilizó un estudio normativo nacional de determinantes cognitivos del envejecimiento saludable,(30) para determinar los pacientes cognitivamente normales.
Caracteristícas de los artículos incluidos
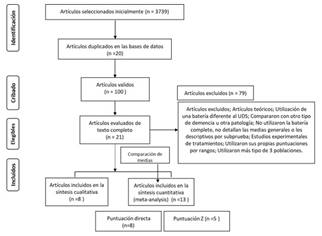
En la revisión sistemática y en la sintesís cualitativa se utilizarón 8 artículos con una muestra de 9260 sujetos; y un rango de edad entre 60 y + 90 años, variable de acuerdo cada estudio, el proceso de selección se puede identificar en la figura 1. De acuerdo a los artículos revisados se ha encontrado que hace apróximadamente 12 años se reportan investigaciones con la UDS.
Se desarrolló una sintesís cuantitativa, donde se incluyeron 13 artículos y se analizaron estadísticamente para generar datos unificados sobre los rendimientos en los subtest de la batería estudiada, donde el proceso de selección se puede identificar a continuación en la Figura 1.
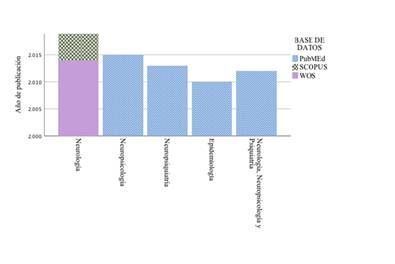
Los resultados de la síntesis cuantitativa arrojan que la muestra analizada es de N=2.8884, pero con un valor promedio de X=2.222; la edad promedio fue 74,1 años y un cociente medial de 15 años de educación. Se evidencia que la base datos científica con mayor cantidad de artículos del tema, fue PubMed/MedLine (X=11). Igualmente se identifica que neurología es el área que mayor número de publicaciones. Tal como se observa en la Figura 2, donde se relaciona el área de conocimiento con mayor publicación sobre la batería.
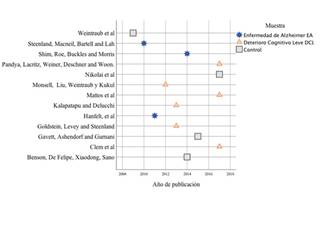
De acuerdo a los artículos seleccionados para el meta-análisis, el mayor número de ellos utilizan población con DCL y Control, tal como se evidencia en la Figura3, donde también se observa una concentración de artículos entre el 2012 y 2017.
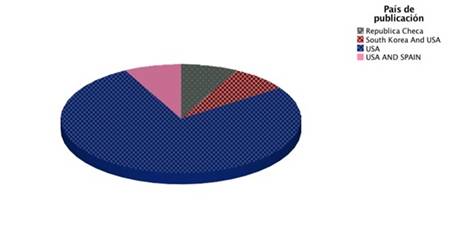
Con respecto a los países de publicación se encontró que Estados Unidos ocupa el primer lugar con un porcentaje de 76,92%. Igualmente se evidencia un 7,69% para paises tales como Republica Checa, Korea Del Sur y España. Sin embargo, Estados Unidos ha participado activamente en el desarrollo de estás investigaciones.Figura 4
Se calculó una comparación de medias para cada subtest de acuerdo a tres categorias, que hacen referncia al tipo de paciente (DTA, DCL o controles). Con respecto a los estudios con temporalidad longitudinal que evidenciaron datos basales, se tomó una única medición de la población. Y artículos de tipo descriptivo-comparativo, se tomó unicamente la muestra clínica (DCL o DTA), lo cual se evidencia en la Tabla 1.
Tabla 1 Comparación de medias generales.
| Normal | DCL (PD) | DCL(Z) | EA | |
| SubTest Uniform Data Set-2 | Media (DE) | Media (DE) | Media (DE) | Media (DE) |
| Examen cognostivo: Minimental | 28,4 (1,3925) | 27,4 (2,15) | 6,1675 | 18,84 (8,14) |
| Prueba de retención dígitos: en orden | 7,9 (2,08) | 7,95 (2,0) | -0,262 (1,07) | 9,92 (8,73) |
| Longitud de la seria correcta más larga: Dígitos en orden | 5,97 (4,67) | - | -0,25 (0,95) | 16,97 (8,29) |
| Prueba de retención dígitos: Orden inverso | 6,03 (2,03) | 5,95 (2,05) | -0,23 (0,97) | 4,915 (1,90) |
| Longitud de la seria correcta más larga: Dígitos en orden inverso | 4,30 (1,17) | - | -0,25 (0,86) | 2,84 (1,54) |
| Memoría Lógica: Recuerdo inmediato | 12,17 ( 3,77) | 9,55 (3,20) | -0,692 (23,71 | 3,28 (3,17) |
| Memoria Lógica: Recuerdo diferido | 10,82 (3,98) | 7,15 (4,8) | -0,82 (2,90) | 1,04 (2,15) |
| Test de Rastreo A | 44,98 (21,89) | 44,05 (20,60) | -0,22 (2,376) | 83,37 (42,38) |
| Test de Rastreo B | 118,13 (60,28) | 129,65 (66,25) | -0,34 (1,45) | 226,95 (83,76) |
| Test de Símbolo y Dígito | 40,57(11,87 | 34,60 (15,30) | -0,34 (1,02) | 20,49 (10,39) |
| Prueba de fluidez verbal: Animales | 19,38 (5,437) | 16,05 (5,05) | -0,59 (0,93) | 6,43 (4,83) |
| Prueba fluidez verbal: Vegetables | 13,15 (3,80) | 11,10 (3,70) | 0,3 (1,19) | 3,77 (3,33) |
| Test de denominación de Boston | 26,62 (3,12) | 24,80 (4,75) | -0,75 (1,35) | 17,34 (7,78) |
*Nota tabla: DE: Desvición Estandar; DCL: Deteriro Cognitivo Leve; EA: Enfermedad de Alzheimer; PD: Puntuación directa; Z: Puntuación Z
DISCUSIÓN
En esta revisión sistemática se incluyeron 8 estudios, los cuales reportan un transcurso desde las primeras investigaciones que se realizaron con el UDS por Morris y cols(9), hasta la última versión de Weintraub y cols.(16) Así muestra una excelente evidencia empírica dentro de las enfermedades neurodegenerativas. Con respecto a la síntesis cuantitativa se utilizaron 13 artículos que permitieron establecer valores mediales con respecto a las puntuaciones directas, de acuerdo a pacientes cognitivamente normales, pacientes con deterioro cognitivo leve y pacientes con demencia de tipo Alzheimer. De acuerdo a dichos resultados, el rendimiento individual en la batería en general está mediado por la edad y los años de educación tanto para angloparlantes,(8)(24) hispano hablantes,(21) como para los Cheslovacos.(20) Con respecto al diagnóstico, Monsell y cols(15) sugieren que las mediciones identifican adecuadamente los estados cognitivos y funcionales de los pacientes, evidenciando sensibilidad para el fenotipo de DCL(18)(31) así como en la detección y caracterización de DTA.(8) Diferentes estudios evidencian también la sensibilidad en la evolución de DCL a demencia y como las puntuaciones especificas del UDS tales como recuerdo diferido, la velocidad de procesamiento y la función global favorecen a la detección de DCL.(31)(23) También, reportan un aumento de compromiso en la prueba de dígitos inversos y el TMT A y B en pacientes con la evolución del tiempo del DCL. A pesar de lo anterior, Pandya y cols(25) en su análisis de reversión y regresión de controles cognitivamente normales y DCL, identificaron el 89% de sensibilidad y 73% de especificidad, mostrando una mejora en el rendimiento cognitivo y una excelente sensibilidad para el diagnóstico de DCL.
En conclusión, la batería neuropsicológica, Uniform Data Set en su V.2, evidencia adecuada precisión diagnóstica para demencia de tipo Alzheimer, y DCL. La versión 3 (UDS-3) promete sensibilidad, especificidad y accesibilidad. Está revisión sistemática mostró que las puntuaciones mediales, representan puntos de cortes, evidenciando diferentes valores mediales para cada tipo de población, permitendo identificar demencia de tipo Alzheimer y deterioro cognitivo leve a través de medias y valores extra de puntuaciones Z para DCL. Por medio de las sub-pruebas que conforman la batería UDS V.2; MMSE, dígitos inversos, memoria lógica inmediata y diferida, test de rastreo A y B, prueba dígito-símbolo, fluidez verbal de animales y de vegetales y la prueba de denominación de Boston, se establecen puntos de corte específicos para demencia tipo Alzheimer. Igualmente, encontramos que la prueba de dígitos directos, evidencia un menor puntaje para pacientes normales, que para pacientes con DTA y discriminan entre sujetos controles y aquellos con deterioro cognitivo leve. Se evidencia una pequeña diferencia para pacientes con DCL con respecto a los pacientes cognitivamente normales.
Las principales limitaciones de este estudio son la heterogeneidad de los estudios y la falta de inclusión de valores para sensibilidad y especificidad de la batería en los estudios empíricos, que evita hacer un metaanálisis de precisión diagnóstica, limitando el estudio a una síntesis cuantitativa de valores de las subpruebas. Este estudio tuvo como fortaleza la inclusión de artículos que tienen homogeneidad en los criterios de diagnóstico utilizados. Los sitios de aplicación son centros de los ADC´s, lo cual es favorable, ya que existen criterios generalizados para estos entornos clínicos, excepto uno que se aplicó en la Republica Checa y, sobre todo, el descriptivo de las sub-pruebas.
La importancia fundamental del UDS es lograr la homogenización, adaptación y estandarización de una serie de datos derivados de pruebas neuropsicológicas comunes y uniformes entre centros de investigación en enfermedad de Alzheimer. Esto permite generar bases comunes o aun diversas, pero comparables a través de datos masivos (big data) en estudios clínicos, genéticos, de biomarcadores diagnósticos y de ensayos terapéuticos para una enfermedad que se ha convertido en la epidemia del siglo.(29) Finalmente, en relación con las posibles líneas de desarrollo en futuras investigaciones, se propone validar la nueva versión de la batería, así como el reporte de datos psicométricos que faciliten estudios meta-analíticos.