Introducción
Los cultivos agrícolas se ven afectados de forma negativa por bacterias, hongos, arvenses, insectos y nematodos, ocasionando reducciones en el rendimiento de las producciones (Thakur y col., 2020). Desde 1960, los métodos de control de plagas agrícolas se realizaban mediante aplicaciones de plaguicidas sintéticos, como el dicloro-difeniltricloroetano (DDT), seguido de otros plaguicidas organofosforados y carbamatos (Kumar, 2012).
Las tecnologías de la revolución verde contribuyeron a aumentar la producción de los alimentos a través de la agricultura intensiva, mediante el uso de fertilizantes químicos y pesticidas (Kumar y Singh, 2015). Sin embargo, los efectos adversos como la degradación de suelos, contaminación del agua, resistencia en los insectos y residuos tóxicos en los alimentos (Lengai y Muthomi, 2018), han impulsado la demanda de producir alimentos saludables, disminuyendo el uso de los recursos naturales, y fortaleciendo la agricultura sostenible (Kumar, ).
La producción de bioplaguicidas microbianos ha tomado un gran auge por la demanda de alimentos libres de químicos, siendo estos esenciales en la agricultura orgánica (Mascarin y Jaronski, 2016). Los bioplaguicidas generalmente están compuestos de bacterias, virus, hongos y nematodos benéficos con actividades quitinolíticas, entomopatógenas y antagonistas, utilizados como controladores biológicos de fitopatógenos, insectos y nematodos fitófagos (Lengai y Muthomi, 2018).
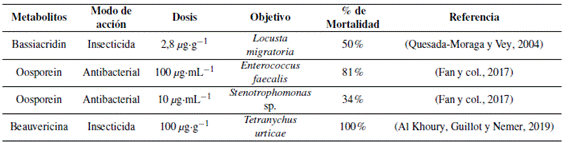
Los análisis bioquímicos y genómicos han demostrado que los metabolitos que producen los microorganismos tienen gran potencial en el control biológico de plagas (Luo y col., 2017). Los metabolitos identificados de Beauveria bassiana son beauvericina y bassiacridin de acción insecticida (Al Khoury, Guillot y Nemer, 2019; Quesada-Moraga y Vey, 2004), y son empleados para el control de Tetranychus urticae, Bemisia tabaci y Locusta migratoria; oosporein con efectos antivirales y antibacteriales en Enterococcus faecalis y Stenotrophomonas spp. (Jeffs y Khachatourians, 1997), y bassianin como inhibidor de la ATP (Patocˇka, 2016).
Las tecnologías de formulación de agentes de control biológico para el escalado comercial deben considerar ciertos criterios para el proceso de producción (Ávila-Hernández y col., 2020) como la estabilización del microorganismo en la etapa de producción, distribución y almacenamiento; también se deben proporcionar las condiciones propicias para la aplicación en campo (Dannon, Dannon y Douro, 2020). Se deben realizar evaluaciones de la persistencia después de la aplicación, y la adaptación a condiciones ambientales sin alterar las propiedades fisicoquímicas del microorganismo (Ávila-Hernández y col., ).
Los plaguicidas elaborados a partir de hongos entomopatógenos se utilizan con frecuencia en los programas fitosanitarios para controlar poblaciones de insectos fitófagos (Luo y col., 2014). Uno de los hongos entomopatógenos con mayor relevancia en el campo agrícola es Beauveria bassiana, empleado para controlar plagas como la broca del café (Hypothenemus hampei), picudo negro en banano (Cosmopolites sordidus), pulgones y arañitas rojas, entre otras (Gerónimo y col., 2016; Al Khoury, Guillot y Nemer, 2019; Ávila-Hernández y col., 2020). Este hongo es considerado un enemigo natural de insectos en los ecosistemas, residuos de cosechas y en los huéspedes colonizados (Marín y col., 2018).
Las formulaciones comerciales de Beauveria bassiana incluyen métodos artesanales como la fermentación en sustratos sólidos, en la cual el hongo se encuentra inoculado en un sustrato y la aplicación se realiza mediante un filtrado de los conidios del microorganismo. En cambio, los métodos más innovadores consisten en desarrollar formulaciones secas y líquidas, impulsando el propágulo del hongo (conidio o blastosporas). El proceso de secado se realiza por aspersión, secado al aire, secado rotativo en tambor al vacío y secado en lecho fluidizado; estas técnicas son empleadas para estabilizar los propágulos de Beauveria bassiana a gran escala y que su vida útil sea satisfactoria (Mascarin y Jaronski, 2016). De acuerdo con el análisis de la problemática del uso de plaguicidas químicos y la necesidad de producir insumos amigables con el medio ambiente, se ha realizado una revisión sistemática que tiene como finalidad describir los procesos de producción de Beauveria bassiana para la formulación de bioplaguicidas de uso agrícola.
Metodología
Se realizó una revisión sistemática de 60 manuscritos en buscadores especializados y bases de datos de ResearchGate (18), Semanticscholar (10), Google Académico (14), Springer (2), SciELO (2), ScienceDirect (6) y PubMed (8), dedicando un tiempo aproximado de 1920 horas en el proceso de búsqueda bibliográfica, revisión y redacción científica. La investigación se enfocó en el entomopatógeno Beauveria bassiana por el potencial biocida para el control de insectos fitófagos, y los procesos de producción in vitro y a escala comercial para la formulación de biopesticidas de uso agrícola. La búsqueda se realizó en revistas como Journal of Applied Entomology, Plant Protection Science, World Journal of Microbiology and Biotechnology, Biology, Journal of Invertebrate Pathology y otras como fuentes primarias; y como fuentes secundarias en instituciones como Servicio Nacional de Sanidad Agraria y empresas que formulan o comercializan insecticidas que contienen Beauveria bassiana. La información seleccionada corresponde a artículos publicados durante los últimos 10 años, con algunas excepciones consideradas por la relevancia aportada a la revisión bibliográfica.
Antecedentes de Beauveria bassiana como controladores biológicos.
El entomopatógeno B. bassiana se observó por primera ocasión en los gusanos de seda, donde las larvas tenían una cubierta de color blanco en el exterior con múltiples inflorescencias que podían contagiar a las larvas sanas en un corto periodo de tiempo (Bassi, 1835). En el año 1954, se reportaron los primeros brotes de infección en acrídidos, pero fue en el año de 1987 cuando se comprobó la patogenicidad del microorganismo en saltamontes bajo condiciones de laboratorio (Inglis, Goettel y Johnson, 1993).
En los últimos años se han descubierto alrededor de 700 especies de insectos hospederos del patógeno B. bassiana (Xiao y col., 2012). Este hongo tiene la capacidad de infectar a los principales taxones de insectos cuando encuentra las condiciones adecuadas para inocular el huésped. Sin embargo, los estudios relacionados con la patogenicidad de B. bassiana se han centrado en los insectos considerados plagas (Meyling y Eilenberg, 2007). La secuencia del genoma de huéspedes infectados demostró que B. bassiana evolucionó a partir de insectos; también se asume que la expresión de ciertos genes de tipo proteasas y quitinasas están asociadas a las funciones necesarias para la patogénesis de insectos y la evolución convergente (Xiao y col., ).
Potencial bioplaguicida de Beauveria bassiana.
Beauveria bassiana es un hongo entomopatógeno utilizado como controlador biológico en plagas de cultivos agrícolas (Barcenilla, 2021). El patógeno ingresa en los insectos a través de los conidios que se adhieren a la cutícula del huésped. La formación del tubo germinativo y el apresorio permite la fijación al tegumento del insecto por presión. La acción de las enzimas hidrolíticas de tipo lipasas, proteasas y quitinasas ingresan al cuerpo del insecto por las partes blandas (Lara-Juache y col., 2021). Las hifas tienen contacto con la hemolinfa que contiene altos contenidos de nutrientes, iniciando una etapa de gemación de blastosporas unicelulares (Mascarin y Jaronski, 2016). El hongo coloniza los tejidos internos del insecto y durante este proceso liberan metabolitos como beauvericina y bassiacridin que ayudan a inhibir el sistema inmunológico, facilitando el ingreso hacia los órganos internos del huésped y provocando su muerte (Figura 1) (Harith-Fadzilah, Abd Ghani y Hassan, 2021). Los insectos infectados muestran una cubierta algodonosa y polvorienta de coloración amarilla cremosa que recubre la parte externa del huésped (Barcenilla, ).
En la etapa de colonización, B. bassiana secreta proteínas y enzimas que pueden ser utilizadas como fábricas celulares para la producción de insumos comerciales. La evaluación de la actividad metabólica, por secuenciación completa del genoma, expresa que B. bassiana posee un pangenoma abierto, con capacidad para colonizar diferentes huéspedes (insectos, nematodos y plantas). Además, se identificaron 10366 genes que codifican para proteínas como proteasas y 145 enzimas activas de carbohidratos de tipo quitinasas, celulasas y hemicelulasas (Vidal y Jaber, 2015).
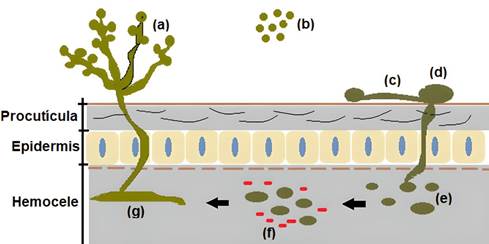
Figura 1 Proceso de infección de Beauveria bassiana en la cutícula de los insectos. (a) Estructuras de B. bassiana (b) Diseminación de conidios B. bassiana. (c) Formación del tubo germinativo en la superficie del cuerpo del insecto. (d) Formación del apresorio e ingreso de la hifa en la procutícula y epidermis. (e) Producción de Blastosporas e invasión en hemocele. (f) Liberación de metabolitos secundarios. (g) Formación de las estructuras del hongo (hifas, micelio y conidios) y liberación al espacio exterior.
La expresión génica de B. bassiana en el proceso de inoculación de insectos demuestran la presencia de enzimas peroxidasas, trehalasa, lipasa, peptidasa, fosfatasa y liasa responsables de la degradación de la cutícula de los huéspedes. Las enzimas quitinasas de B. bassiana hidrolizan los enlaces b de polímeros de quitina en monómeros de N-acetil b-D-glucosamina presentes en el exoesqueleto de artrópodos (Amobonye y col., 2020). La cutícula de los insectos está formada por lípidos superficiales que actúan como una barrera protectora de patógenos. Sin embargo, las lipasas producidas por B. bassiana contribuyen a la degradación de la cutícula del insecto (Salazar y col., 2020); estas son enzimas solubles en agua que actúan sobre sustratos insolubles que tienen la capacidad de hidrolizar triglicéridos y transformarlos a ácidos grasos y glicerol. Las proteasas entomopatógenas actúan sobre la cutícula del huésped y atacan el tejido debilitado por acciones quitinolíticas (Amobonye y col., ).
La diversidad de toxinas producidas por B. bassiana puede ir desde compuestos simples como las macromoléculas biológicas, por ejemplo, ácido oxálico, 2,6piridindicarboxílico (ácido dipicolínico), y compuestos de estructuras más complejas de naturaleza peptídica cíclica y lineal como beauvericina, bassiacridina, beauverólidos y bassianólidos (Borges y col., 2010). Las toxinas alteran la permeabilidad natural y artificial de las membranas, inducen la pérdida de líquidos de las células, producen cambios en el núcleo durante los procesos de la muda y metamorfosis, deforman las estructuras externas de los insectos e interfieren en los procesos de fecundación (Patocˇka, 2016). Por último, las enzimas lipasas, quitinasas, proteasas y amilasas degradan el exoesqueleto del huésped y permite el ingreso del hongo en sus tejidos internos (Cortés y Mosqueda, 2013).
Producción in vitro de Beauveria bassiana
Los procesos de producción de conidios de B. bassiana pueden ir desde métodos muy simples a procesos que implican mayor tecnificación (Vela y col., 2019). El primer paso para la producción de B. bassiana consiste en realizar aislamiento de las cepas del microorganismo; para ello es importante determinar la composición del medio de cultivo y los parámetros óptimos para el crecimiento. Greenfield y col. (2016) afirma que las cepas de B. bassiana pueden cultivarse en agar glucosa, peptona de soya, agar papa-dextrosa (PDA), agar de dextrosa-Sabouraud (SDA) o agar harina de avena. Las temperaturas óptimas para el crecimiento van desde 22-26 ◦C, alternando luz y oscuridad por ocho días.
En cambio, Bugti y col. (2018) manifiestan que se debe realizar una suspensión de esporas del microorganismo e inocular el medio de cultivo agar dextrosa-Sabouraud (agar 20 g, peptona 10 g, dextrosa 40 g, potasio 0.5 mg, en 1000 mL de agua destilada) e incubar a 24 ± 1 ◦C por doce días.
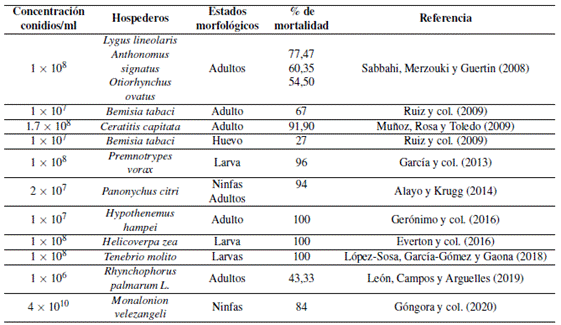
El segundo paso consiste en comprobar la patogenicidad de B. bassiana a través de inoculaciones de insectos sanos. Para ello se debe preparar suspensiones de conidios en una solución de Tween 80 al 0.05 %, con agitación constante por cinco minutos, y ajustar la concentración de esporas y rociar los insectos (Bugti y col., 2018). En la Tabla 1 se detallan estudios realizados para comprobar la patogénesis de B. bassiana en diferentes huéspedes.
Fermentaciones en sustratos sólidos
La producción de Beauveria bassiana en sustratos sólidos por reproducción de conidios aéreos es el método más utilizado a nivel comercial tanto para pequeñas, medianas y grandes empresas dedicadas a la producción de bioplaguicidas (Feng, Poprawski y Khachatourians, 2008). Los medios de cultivo para la producción de B. bassiana deben tener una composición de nutrientes y condiciones controladas de pH, temperatura, luz, disponibilidad de agua y mezcla de gases atmosféricos, pues son factores cruciales para el crecimiento del microorganismo y esporulación (Patocˇka, 2016). El proceso de producción consiste en inocular conidios de B. bassiana en sustratos sólidos nutritivos. La fermentación en sustratos sólidos bajo condiciones controladas pueden alcanzar rendimientos desde 4 × 1012 a 4 × 1013 conidios·kg−1.
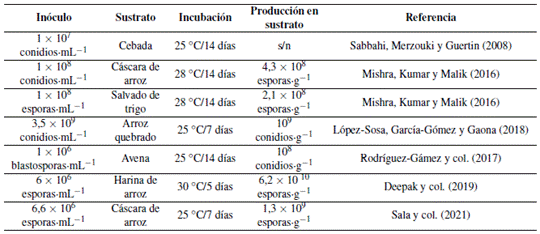
Los materiales más utilizados para la fermentación en estado sólido es el arroz, cebada, trigo, centeno, sorgo y maíz, (Jaronski, 2014). Así mismo, los desechos agroindustriales permiten reducir los costos de producción y consumo de energía. Un ejemplo de ello es la piel de papa y cáscara de arroz, en condiciones óptimas de humedad 65-70 %, temperatura 25 ◦C y tiempo entre 7 a 8 días, permite alcanzar una producción de 1.3 × 109 esporas·g−1 de B. bassiana (Sala y col., 2021).
Tabla 1 Estudios realizados para comprobar la patogénesis de Beauveria bassiana en diferentes hospederos y su porcentaje de mortalidad
Otro factor importante son los contenedores de fermentación, estos pueden ser bolsas de plásticos resistentes a altas temperaturas o grandes cámaras, considerando la aireación ya que los propágulos requieren de un equilibrado intercambio de gases para el crecimiento micelial. La producción de conidios aéreos se puede realizar a través de una o dos etapas. La primera etapa consiste en realizar la inoculación del hongo directamente del sustrato sólido y la segunda etapa implica la producción del inóculo por fermentación líquida y posterior la inoculación en el sustrato sólido (Mascarin y Jaronski, 2016).
El sustrato debe estar previamente esterilizado a 121 ◦C, 15 lb de presión por 30 minutos, se inocula el sustrato con la suspensión de conidios de B. bassiana o con una proporción de micelio. Los sustratos inoculados se incuban a 25 ◦C por 7 días y se eliminan los sustratos contaminados (López-Sosa, García-Gómez y Gaona, 2018). Por consiguiente, las bolsas se agitan para oxigenar el inóculo y conseguir una mezcla homogénea, se incuba por 21 días a 24 ◦C (Monzón, 2001) conservando una humedad relativa del 53 %. Una vez esporulado el hongo en todo el sustrato, se realiza el proceso de secado a temperaturas entre 16-20 ◦C por un periodo de 5 a 6 días para reducir la humedad relativa al 15 % (Gómez y col., ).
El problema principal de la fermentación sólida es el escalado comercial, siendo el principal enfoque la producción de un gran número de conidios de forma eficiente y económica para reducir los costos de producción y poder competir con los plaguicidas tradicionales (Rodríguez-Gámez y col., 2017). Por ello es importante utilizar sustratos y recipientes de buena calidad, pero al mismo tiempo económicos; y, además, vigilar de forma constante cada uno de los procesos de producción para evitar contaminaciones, realizando un correcto proceso de esterilización y manipulación de los materiales. Los sustratos y las condiciones ambientales para la fermentación sólida de Beauveria bassiana se muestran en la Tabla 2.
Fermentaciones en sustratos líquidos
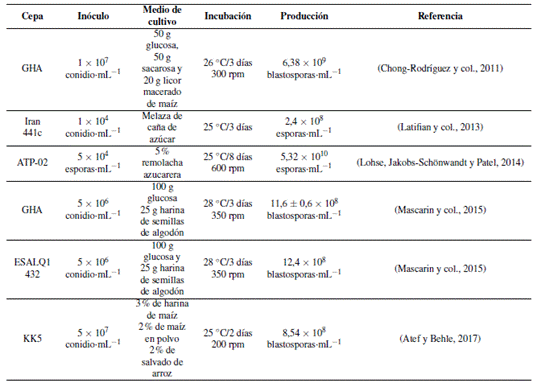
El proceso de fermentación líquida facilita el escalado masivo para la formulación de bioplaguicidas. Este método permite tener un mejor control de las variables ambientales y reducir los tiempos de producción (Jaronski, 2014). Sin embargo, la implementación a escala comercial requiere de una considerable inversión en equipamiento para la producción masiva de micoinsecticidas, y es uno de los métodos más aplicados a escala comercial (Mascarin y Jaronski, 2016).
La fermentación líquida se puede realizar de forma estacionaria o por fermentación sumergida. La primera produce micelios y conidios aéreos, por el contrario, la segunda opción produce blastosporas, conidios de microciclo, o microesclerocios en un medio líquido agitado y aireado (Jaronski, 2014). Los medios de cultivo deben ser ricos en nutrientes con altas concentraciones de carbono y nitrógeno para inducir la producción de blastosporas o conidios. Una relación de C:N óptima induce el crecimiento del hongo bajo condiciones controladas (Pham y col., 2009).
Según García y col. (2013) el medio de cultivo SDA (Sabouraud dextrose agar) proporciona nutrientes adecuados para el desarrollo de B. bassiana en un periodo de incubación de 15 días a 30 ◦C. Así mismo, Pham y col. (2009) señalan que los inóculos de conidios para medios de cultivos líquidos se deben obtener a partir de cultivos esporulados de dos semanas de edad en Agar Papa Dextrosa (PDA) a una temperatura de 25 ± 1 ◦C. La cosecha de los conidios se realiza mediante un raspado del inóculo con una solución de tween 80 al 0,02 % (Lee y col., 2016). Se inoculan los matraces que contiene medio de cultivo líquido con melaza como fuente de carbono (García y col., ), caldo de levadura o glucosa por 6 días a una temperatura de 24-26 ◦C (Lee y col., ) en un agitador rotatorio a 200 rpm hasta conseguir una suspensión estable (Pham y col., ). La suspensión obtenida se utiliza para inocular el fermentador en una concentración del 10 % referente al volumen del fermentador, con una fase de propagación de 4 días hasta que el hongo alcance el 80 % de la fase logarítmica de crecimiento (García y col., ).
Los sustratos utilizados para la elaboración de los medios de cultivos líquidos deben ser de bajos costos, y al mismo tiempo deben proporcionar las condiciones adecuadas para la producción de blastosporas o conidios (Mascarin y col., 2015). En este contexto, Pham y col. (2009) comunica que un medio de cultivo con harina de maíz al 3 %, polvo de maceración de maíz 2 % y de salvado de arroz 2 % permite obtener una producción de 8,54 × 108 blastosporas·mL−1. En cambio, García y col. (2013) informa que para la producción de blastosporas el medio óptimo debe tener melaza 14,5mL·L−1, (NH4)2 SO4 6 g·L−1, KH2PO4 3,5 g·L−1, MgSO4 0,5 g·L−1, NaCl 0,1g·L−1, CaCl2 0,1g·L−1, y se puede obtener una producción 8,40 × 108 blastosporas·mL−1. Por otro lado, Elías-Santos y col. (2021) informa que un medio de cultivo con 20 g de harina de pericarpio de cacahuate y 200 g de glucosa de maíz permite obtener 5,10 × 108 blastosporas·mL−1.
De igual forma, las condiciones ambientales son importantes para la producción Beauveria bassiana en medios de cultivos sumergidos. El rango de temperatura se sitúa ente los 25-30 ◦C, pH del medio de cultivo 5.4, agitación constante de 200 a 400 rpm, hasta que el hongo pueda alcanzar el 80 % de la fase logarítmica de crecimiento (Pham y col., 2009; García y col., 2013; Elías-Santos y col., 2021). En la Tabla 3 se pueden observar los medios de cultivos y las condiciones ambientales para la producción de B. bassiana por fermentación de sustratos líquidos.
Producción de metabolitos secundarios de Beauveria bassiana
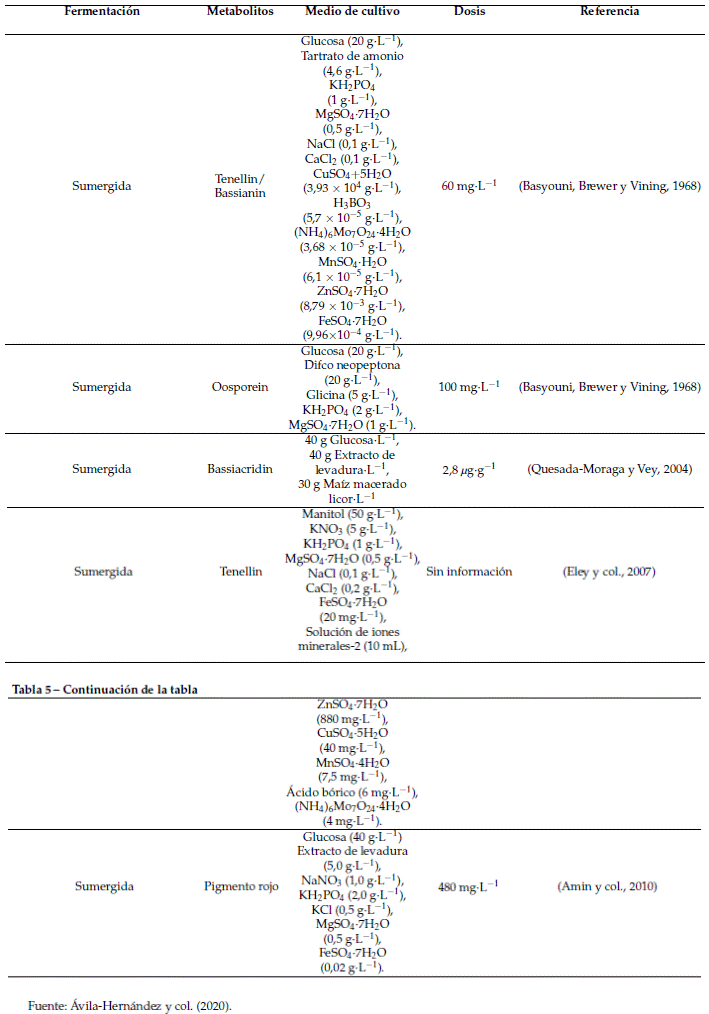
El entomopatógeno Beauveria bassiana secreta una gran variedad de enzimas y metabolitos biológicamente activos (Amobonye y col., 2020), con potenciales de aplicación en los sectores industriales, agrícolas y farmacéuticos, entre otros (MancillasParedes y col., ). Las enzimas más importantes producidas por B. bassiana son las quitinasas, lipasas y proteasas, aunque también producen amilasa, asparaginasa, celulasa, galactosidasa, etc. (Amobonye y col., ); y metabolitos con actividad insecticida (Tabla 4) como beauvericina (Al Khoury, Guillot y Nemer, 2019), bassiacridin (Quesada-Moraga y Vey, 2004), bassianolide (Patocˇka, 2016), antivirales y antibacteriales como oosporein (Jeffs y Khachatourians, 1997), y bassianin como inhibidor de la ATP (Patocˇka, ). La producción de metabolitos secundarios está influenciada por las condiciones ambientales y nutrientes disponibles en el medio de cultivo (Ávila-Hernández y col., 2020) (Tabla 5).
Aplicación de bioplaguicidas en la agricultura
El crecimiento poblacional, la degradación del medio ambiente (Thakur y col., 2020), la demanda de cultivos libres de químicos y las estrictas regulaciones de los plaguicidas en países europeos y norte de América (Mascarin y Jaronski, 2016) representan un desafío para la producción de alimentos en todo el mundo. La agricultura convencional depende de los plaguicidas para el manejo integrado de plagas y enfermedades en los cultivos agrícolas. Una alternativa que contribuye a reducir la incidencia de fitófagos o fitopatógenos son los bioplaguicidas formulados a través de la reproducción de microorganismos benéficos o la producción de metabolitos con actividades insecticidas, fungicidas o bactericida (Tabla 6). Las ventajas que poseen estos formulados es que se degradan de forma natural en el ambiente, no almacenan residuos en los tejidos vegetales, no crean resistencias hacia los activos que producen, y disminuyen la presencia de enemigos naturales en los cultivos (Thakur y col., ).
La creciente aceptación de los productos biológicos ha permitido desarrollar formulaciones a partir de hongos entomopatógenos, por fermentaciones sólidas, líquidas, bifásicas y metabolitos secundarios. En la actualidad, se utilizan con frecuencia en los programas fitosanitarios de los cultivos agrícolas para controlar poblaciones de insectos fitófagos (Luo y col., 2014). La actividad insecticida de B. bassiana es más rápida en relación con otros microorganismos entomopatógenos, y los conidios pueden persistir por más tiempo en el ambiente. Además, Sabbahi, Merzouki y Guertin (2008) afirma que las posibilidades de adquirir resistencia por parte de los insectos hacia B. bassiana es nula, debido a los diferentes modos de acción que el hongo utiliza para invadir el cuerpo de los huéspedes, y al ser un organismo vivo puede adaptarse a los cambios del hospedador.
Tabla 5 Medios de cultivos formulados para la producción de metabolitos secundarios de Beauveria bassiana.
La eficacia del bioplaguicida Beauveria bassiana depende de la integración en los programas de manejo integrado de plagas para potenciar la eficacia en el control de insectos (Mascarin y Jaronski, 2016). Si bien B. bassiana es un microorganismo eficaz para el control biológico de insectos, las condiciones ambientales juegan un papel importante en el mecanismo de acción del entomopatógeno, por ello resulta indispensable desarrollar nuevas tecnologías para la producción de los compuestos activos, que potencien las formulaciones de biopesticidas.
Conclusiones
Contribución de los autores
La elaboración de biopesticidas a base de Beauveria bassiana se puede realizar a través de fermentaciones sólidas y líquidas. El primer protocolo ha sido ampliamente utilizado debido que requiere una baja inversión en equipamientos y no se emplean protocolos complejos en la producción y formulación. Sin embargo, es necesario emplear un sustrato de bajo costo y controlar exhaustivamente las fases de cada proceso para evitar eventos de contaminación. Por otro lado, la fermentación líquida permite ejercer un mayor control de las variables ambientales, reduce los tiempos de producción, pero la implementación a escala comercial requiere de una considerable inversión en equipamiento para la producción masiva de micoinsecticidas.
Para los procesos de fermentación es necesario controlar las variables ambientales, ya que estos factores influyen en la producción de esporas y blastosporas. Las condiciones óptimas consisten en mantener una temperatura de 25 ◦C, humedad relativa de 65 a 70 %, pH de 5.4, tiempo de propagación entre 4 a 8 días, y solo para el proceso de fermentación líquida el inóculo requiere de agitación constante entre 200 a 400 rpm.
{ label (or @symbol) needed for fn[@id='fn1'] }.