Forma sugerida de citar:
Hernández-Amasifuen, A., Argüelles-Curaca, A., Cortez-Lázaro, A.A. y Díaz-Pillasca, H.B. (2021). Inducción in vitro de callos a partir de explantes foliares en rocoto (Capsicum pubescens Ruiz & Pav.). La Granja: Revista de Ciencias de la Vida. Vol. 34(2):131-140. http://doi.org/10.17163/lgr.n34.2021.09.
1. Introducción
El rocoto (Capsicum pubescens Ruiz & Pav.) es una planta herbácea con ciclo de vida perenne que pertenece a la familia Solanaceae. Su centro de origen es la región andina de Perú, siendo posible encontrarse de manera silvestre en la sierra y selva alta. Esta especie se diferencia de las demás especies que pertenecen al género Capsicum por presentar flores con coloración púrpura o morada y por sus semillas de color negro. El fruto puede variar en forma, tamaño y color, pero se caracteriza por su picor y por esta razón es muy empleado en la gastronomía peruana. Además, el rocoto presenta propiedades farmacéuticas y medicinales, relacionadas a la capsaicina (Caballero, Márquez y Albero, 2017).
En Perú se han definido dos variedades de rocoto, el rocoto de monte y el rocoto de huerta o serrano. El rocoto de monte es denominado de esta manera por ser cultivado en mayor parte en la selva central, presenta mayor tamaño de fruto, por lo cual existe una mayor demanda de esta variedad para la preparación del rocoto relleno. La otra variedad es el rocoto de huerta o serrano, cultivado en todas las regiones del país, mayormente en los valles andinos. El fruto de esta variedad es de menor tamaño, pero con un característico picor fuerte que se utiliza para salsas (Valdez, 2017).
La producción nacional de rocoto ha ido incrementando con una tasa anual del 5% principalmente por la gran demanda gastronómica que se viene desarrollando en país; debido a esto se considera en la actualidad como un producto de importancia nacional (Sardón, 2015). Pero también se debe considerar que este cultivo presenta susceptibilidad a la marchitez, pudrición radicular y entre otras enfermedades causadas por Fusarium oxysporum, Phytoptora capsici, Risotonia solanacearum y entre otros fitopatógenos. También es susceptible a daños causados por virus que pueden llegar a causar amarrillamiento en las nervaduras, deformaciones en hojas y frutos, enanismo, falta de vigor y caída de las hojas. La principal causa de la diseminación de estas enfermedades son las semillas provenientes de cultivares o almácigos infectados, debido que en este cultivo normalmente se emplean semillas de campañas o sembríos anteriores, y en el caso de algunos virus se diseminan al contacto entre plantas (Lucana, 2012; Hernández, Pineda y Noriega, 2019).
Es importante fortalecer la cadena de valor del rocoto, razón por la cual se busca obtener semillas de calidad y certificadas, o plántulas libres de patógenos para poder mantener cultivos más uniformes que presenten mayor calidad y producción. Dentro de las alternativas para la obtención de material vegetal aséptico se consideran a las herramientas biotecnológicas, con el empleo de técnicas de cultivo de tejidos vegetales in vitro (Robledo y Carrillo, 2004; Sanatombi y Sharma, 2007; Orlinska y Nowaczyk, 2015). Estas técnicas permiten la proliferación de células a partir de un explante (fragmento vegetal que puede ser meristemos, yemas axilares, hojas, raíces, anteras e incluso microsporas) en un medio de cultivo provisto de nutrientes, vitaminas, y en algunos casos también de hormonas (Levitus et al., 2010; Vélez et al., 2010; Venkataiah et al., 2016). Estos explantes, en condiciones apropiadas, inducirán a la formación de callos, que son masas amorfas o desorganizadas de células indiferenciadas. La importancia del callo radica en su funcionalidad de crecimiento irregular con potencial para formar órganos o embriones en las condiciones adecuadas (Alayón et al., 2006; Pérez et al., 2009; Terra et al., 2009; Smith, 2012; Rashmi y Trivedi, 2014).
El potencial de los callos como vía para la organogénesis y embriogénesis indirecta es una alternativa para programas de mejoramiento genético en rocoto, debido a que estos métodos en algunas especies o genotipos al ser introducidos en medios de cultivo in vitro con diferentes concentraciones de fitohormonas o combinaciones de estas pueden inducir a variación somaclonal, permitiendo obtener nuevas características o la eliminación de alguna indeseada (Sala y Labra, 2003; Rodríguez et al., 2014). Pero de no presentarse estas variaciones somaclonales se pueden multiplicar genotipos prometedores de buen rendimiento y buena calidad, como se viene desarrollando en el cultivo de tejidos vegetales in vitro en diferentes especies del género Capsicum (Marín, 2012; Gómez, 2016; Gutierrez-Rosati y Vega, 2017; Izquierdo, Alcaraz y Rodríguez-Álvarez, 2017).
Por lo tanto, la presente investigación se planteó el objetivo de desarrollar una metodología para la inducción de callos in vitro a partir de segmentos de hojas en rocoto.
2. Materiales y Métodos
La presente investigación se realizó en las instalaciones del laboratorio de Biotecnología Vegetal de la Escuela Profesional de Biología con mención en Biotecnología, ubicada en la Universidad Nacional José Faustino Sánchez Carrión, Huacho, Lima, Perú.
2. 1. Desinfección del material vegetal
Se emplearon semillas de rocoto obtenidas a partir de frutos de rocotos maduros presentes en el invernadero perteneciente al laboratorio. Se lavaron las semillas con agua más detergente comercial durante 5 minutos, y luego se continuó con el proceso de desinfección en cámara de flujo laminar empleando el protocolo establecido por Hernández, Pineda y Díaz (2019). Primero se sumergieron las semillas en etanol al 70% durante 1 minuto, luego se sumergieron en una solución de hipoclorito de sodio al 2% durante 15 minutos en agitación constante. Transcurrido el tiempo se realizaron tres enjuagues con agua destilada estéril, luego fueron coladas en papel filtro y se colocaron tres semillas por tubo de ensayo con medio de cultivo MS (Murashige y Skoog, 1962). Todos los tratamientos se mantuvieron en cámara de crecimiento (Plant Growth Chamber, LGC – 5201 G, LabTech) en condiciones de oscuridad total a 25 °C, con humedad relativa del 75 ± 2%. Cuando inició la germinación se cambiaron a fotoperiodo de 16 horas de luz y 8 horas de oscuridad.
El medio de cultivo MS estuvo constituido por las sales descritas por Murashige y Skoog (1962), adicionado con mioinositol (100 mg l−1), ácido nicotínico (0,5 mg l−1), piridoxina HCL (0,5 mg l−1), tiamina HCL (0,1 mg l−1), glicina (2 mg l−1) y sacarosa (30 g l−1), antes de agregar el agar agar (7 g l−1) se ajustó el pH a 5,7 ± 0,1 empleando el potenciómetro Lab 850 (SI Analytics). Posteriormente se procedió a esterilizar en autoclave (BKM-Z18N, Biobase) a 1,2 Bar de presión y 121 °C durante 20 minutos.
2.2. Inducción de callos
De las plántulas germinadas in vitro se seleccionaron las dos primeras hojas verdaderas, las cuales fueron segmentadas en explantes de 1 cm y se introdujeron cinco segmentos por medio de cultivo MS, adicionado con mioinositol (100 mg l−1), ácido nicotínico (0,5 mg l−1), piridoxina HCL (0,5 mg l−1), tiamina HCL (0,1 mg l−1), glicina (2 mg l−1) sacarosa (30 g l−1) y la auxina 2,4-D en diferentes concentraciones (Tabla 1), seguidamente se ajustó el pH a 5,7 ± 0,1 y se agregó agar agar (7 g l−1). Posteriormente se esterilizó en autoclave a 1,2 Bar de presión y 121 °C durante 20 minutos. Todos los tratamientos se mantuvieron en cámara de crecimiento (Plant Growth Chamber, LGC – 5201 G, LabTech) en condiciones de oscuridad total a 25 °C y con humedad relativa del 75 ± 2% durante 35 días, con observaciones cada siete días para diferenciar el progreso de inducción.
2.3. Diseño experimental y análisis estadístico
El diseño fue completamente al azar (DCA) para cinco tratamientos, utilizándose 15 repeticiones por tratamiento; la unidad experimental está constituida por cada segmento de hoja de rocoto. Se evaluó el porcentaje de inducción de callos en hojas de rocoto y el grado de los callos en la escala de Santana (1982) (Tabla 2). Los datos obtenidos se sometieron a Análisis de Varianza (ANVA) y comparación entre las medias con prueba de Tukey (p ≤ 0,05); ambos análisis se realizaron con el paquete estadístico agricolae del programa R (versión 4.0.3 para Windows).
3. Resultados
La metodología empleada para la desinfección de semillas de rocoto permitió obtener 100% de semillas libres de contaminación en los medios de cultivo, permitiendo la germinación sin problemas por bacterias u hongos que compitan con la plántula en crecimiento.
La inducción de callos a partir de explantes foliares en rocoto se logró apreciar desde el séptimo día en los tratamientos adicionados con 0,75 y 1 mg l−1 de 2,4-D (T4 y T5, respectivamente) formando callos de grado 1. Los tratamientos adicionados con 0,25 y 0,5 mg l−1 de 2,4-D presentaron la formación de callos en las hojas de rocoto en el transcurso de la segunda semana de introducción en los medios de inducción. Transcurrido los 35 días, los medios de cultivo MS adicionados con 0,75 y 1 mg l−1 de 2,4-D presentaron los mayores porcentajes de formación de callos con 100% de inducción de callos en hojas de rocoto (Figura 1), presentando diferencias significativas con los demás tratamientos (Figura 2).
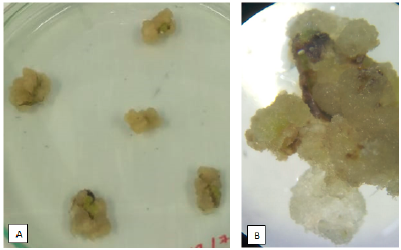
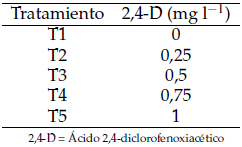
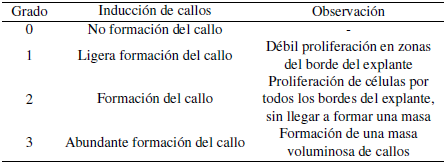
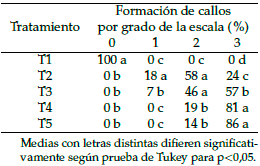
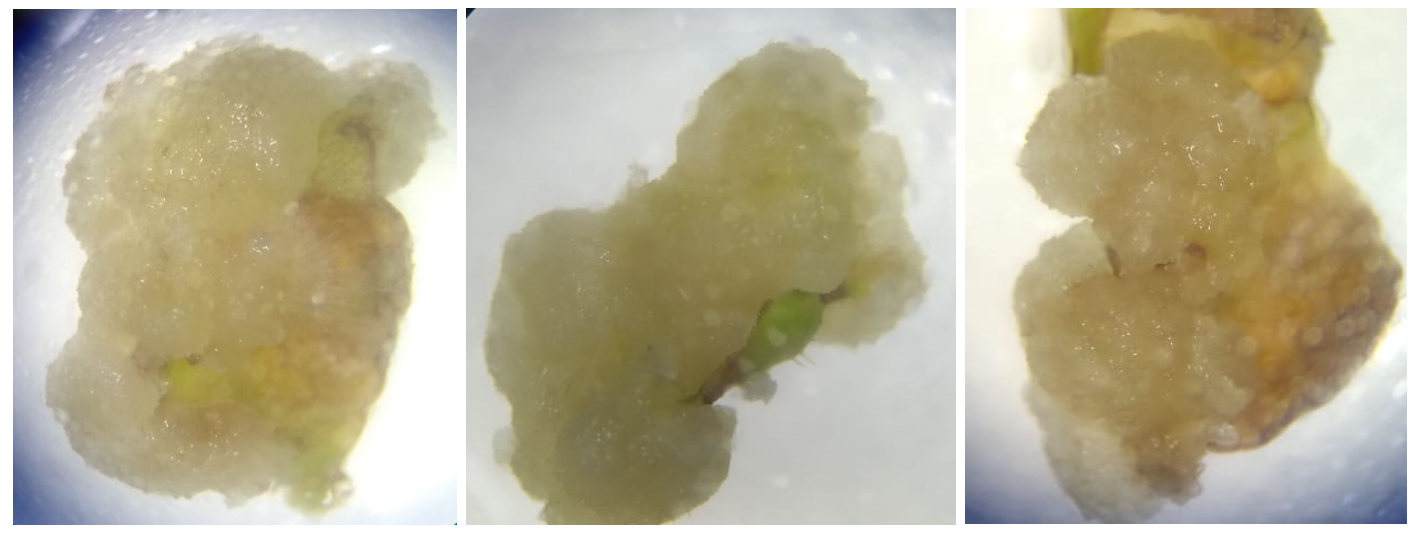
Figura 1. A. Callos a los 35 días formados a partir de hojas de rocoto en medio basal MS con 0,75 mg l−1 de 2,4-D. B. Callo inducido a los 35 días con el tratamiento 1 mg l−1 de 2,4-D con coloración crema, zonas translucidas y de consistencia friable.
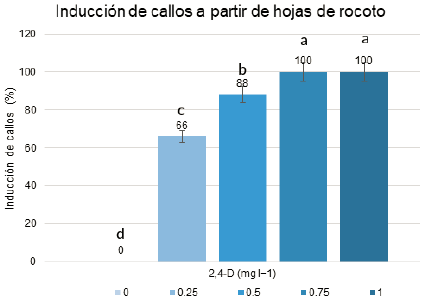
Figura 2. Porcentaje de inducción de callos in vitro a partir de hojas de rocoto. Medias con letras distintas difieren significativamente según prueba de Tukey para p<0,05
Los tratamientos con mayores porcentajes de callos de grado 3 fueron los medios de cultivo MS de 0,75 y 1 mg l−1 de 2,4-D con 81% y 86%, respectivamente; sin embargo, no hubo diferencias significativas entre ambos tratamientos (Tabla 3). Seguidos del tratamiento de 0,5 mg l−1 de 2,4-D con 57%, mientras que el tratamiento de 0,25 mg l−1 de 2,4-D presentó mayor porcentaje de callos pertenecientes al grado 2.
Las características morfológicas de los callos fueron de color crema amarillo y en algunos explantes presentaron zonas blanquecinas o translucidas, y la consistencia de los callos fue friable. Los callos iniciaron su formación en los sitios de corte (bordes) de los explantes, llegando a cubrir por completo la superficie de los explantes en los tratamientos T3 y T4. Por lo que se puede indicar que el rocoto tiene buena respuesta a la inducción de callos, en rápida formación y crecimiento (Figura 3).
4. Discusión
Se logró inducir en los explantes foliares de rocoto la formación de callos in vitro con los medios de cultivo MS con presencia de 2,4-D, la apariencia de los callos fue translucida y compacta. La inducción de callos a partir de hojas dentro del género Capsicum es muy favorable en comparación a otros tipos de explantes (Solís-Ramos et al., 2010; Alva-Guzmán, Cerna-Rebaza y Chico-Ruíz, 2014; Argüelles et al., 2020). Tal como afirma Rodríguez et al. (2014) y Espinosa et al. (2012), la inducción de callos en el caso de las hojas es altamente dependiente del tipo de explante y hormona empleada, y a diferencia de otros explantes, se ve un claro incremento de callos cuando se aumenta la concentración de 2,4-D, además de que este tipo de hormona influye en el aspecto de los callos.
La adición de auxinas y su concentración en el medio de cultivo puede generar un mayor porcentaje de inducción de callos dependiendo de la especie o genotipo empleado, pero la acción de las auxinas está relacionada a la presencia de compuestos presentes en el medio de cultivo que tienen mayor influencia en el desarrollo y diferenciación celular (Feeney et al., 2007; Meiners, Schwab y Szankowski, 2007). Esto debido a que en el cultivo in vitro estos compuestos endógenos presentan cambios drásticos en el ambiente celular, lo que genera efecto de estrés que puede causar una reorganización celular y formar una masa de células no diferenciadas (Fehér, Pasternak y Dudits, 2003; Shiram, Kumar y Shitole, 2008).
Los callos que se fueron generando en las primeras semanas iniciaron en los bordes de los explantes, y progresaron gradualmente en el explante con el transcurso de los días. En el día 35 los explantes se encontraban cubiertos y hubo un incremento en el tamaño de los callos. Smith (2012), afirma que los callos se generan a partir de la zona de corte de los explantes, zona que está en contacto directo al medio con los reguladores de crecimiento que influyen en una acumulación de auxinas, estimulando una continua división mitótica que genera la formación de tejido calloso poco a poco hasta cubrir el explante en gran parte o por completo.
El efecto de la auxina 2,4-D sobre los explantes foliares de rocoto resultó en la inducción de callos, lo que podría estar relacionado a las acciones fisiológicas que se activan en el explante por medio de la auxina exógena adicionada en el medio de cultivo. Taiz y Zieger (1998), determinaron que la inducción se expresa por medio de genes que codifican factores proteicos mediante la unión de las auxinas a receptores externos e internos. Azcón-Bieto y Talón (2008), descubrieron que los factores proteicos permiten el aumento de la plasticidad y ablandamiento de la pared celular, resultando en la dilatación de la célula por presión de turgencia, incrementando de tamaño hasta que la pared celular opone resistencia. Pero también la inducción de callos está influenciada por enzimas que activan o reprimen la transcripción de genes que median las acciones fisiológicas de las citoquininas; estas enzimas son las histidinas fosfotransferasas, las cuales son activadas por la unión de las citoquininas a receptores tipo histidina quinasas (Müller y Sheen, 2007).
La formación de los callos de rocoto en la primera semana puede ser un hallazgo de importancia porque brinda información de ser una especie de rápido efecto de inducción. Los resultados obtenidos fueron superiores en comparación con los obtenidos por Alva-Guzmán, Cerna-Rebaza y Chico-Ruíz (2014), quienes generaron callos en Capsicum chinensis a partir del décimo día de introducción del explante al medio de inducción, empleando 0,5 y 1 mg l−1 de 2,4-D.
Se resalta la importancia de la auxina 2,4-D, por ser la principal fitohormona empleada en condiciones in vitro para la inducción de callos, existiendo un gran número de reportes de su adición en los medios de cultivo, tanto para especies del mismo género que el rocoto como para otros géneros (Larson et al., 2006; Gómez y Ríos, 2006; Terra et al., 2009; Hernández y Díaz, 2019, Hernández et al., 2020).
También se debe tener en cuenta la edad de los explantes empleados, siendo las primeras hojas verdaderas de rocoto las que influenciaron en el estudio al presentar un mayor potencial de inducción, tal como afirman Alleweldt y Radler (1962), al indicar que la edad fisiológica de los explantes es inversamente proporcional a su potencial organogénico.
Estos resultados suponen un avance importante en la aplicación de técnicas biotecnológicas en programas de mejoramiento genético de rocoto, presentándose de manera favorable para el potencial uso de callos de esta especie en cultivos celulares para la obtención de metabolitos secundarios de interés farmacológico. De igual forma, es una base para futuras investigaciones en inducción de embriogénesis somática indirecta, organogénesis indirecta, rizogénsis, aislamiento de protoplastos, entre otros.